主编推荐 ‖ 基于艰难梭菌tcdC基因的新型LAMP检测方法的研发及临床诊断效能评估
2025-05-08 中国感染控制杂志 中国感染控制杂志 发表于陕西省
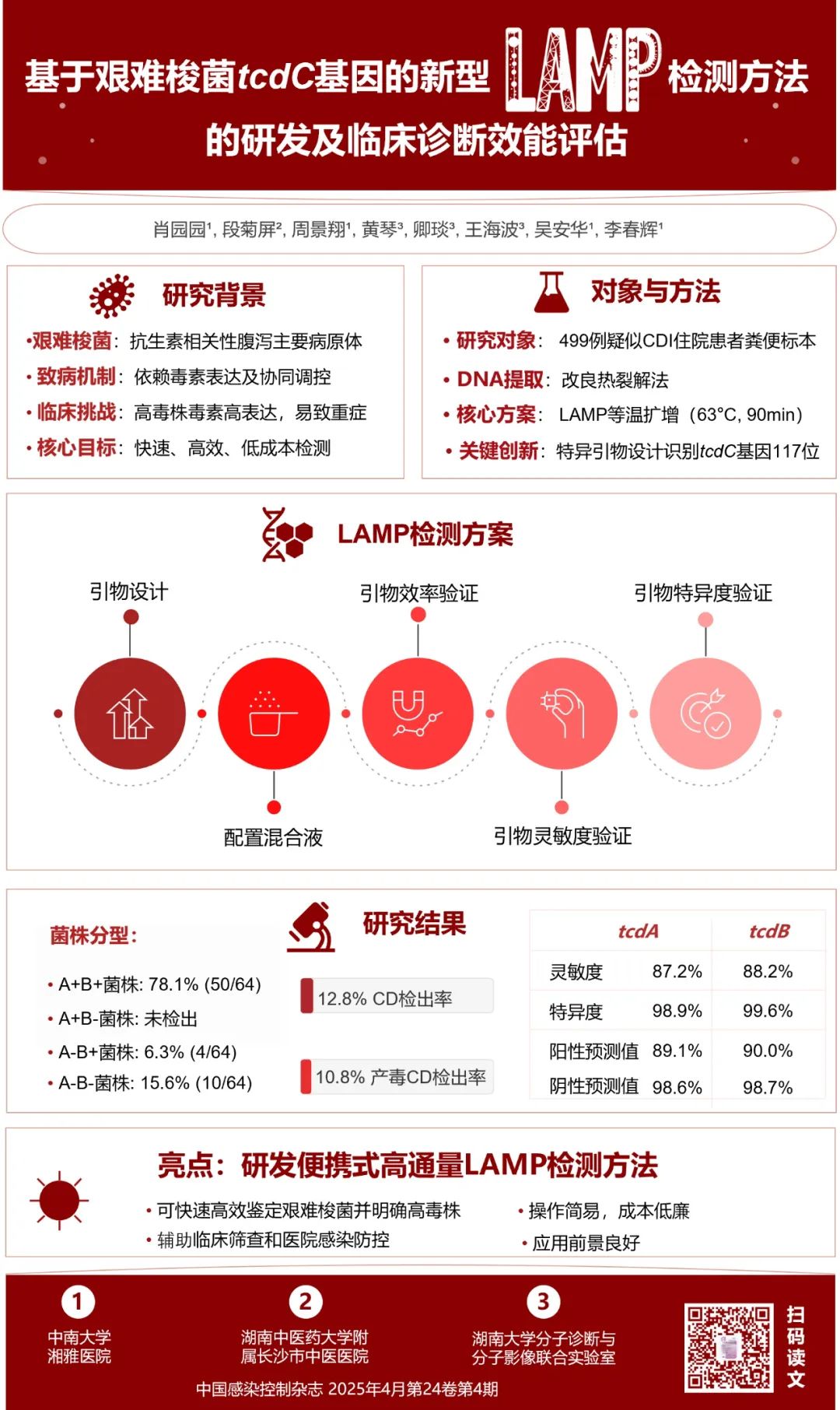
本便携式高通量LAMP检测方法能快速、高效鉴定艰难梭菌并且明确高毒株。
导 读
艰难梭菌(Clostridioides difficile, CD)是抗生素相关性腹泻(antibiotic-associated diarrhea, AAD)的主要病原体,已成为全球医院获得性腹泻最常见的病原体之一。CD致病性取决于毒素表达:产毒株可分泌毒素A(tcdA编码)、毒素B(tcdB编码)及二元毒素,其中tcdA/B受致病决定区内tcdC(负调控)、tcdD(正调控)及tcdE(膜孔蛋白)协同调控。RT027高毒株因毒素高表达易引发重症,临床表现为腹泻、假膜性肠炎,严重者可进展为中毒性巨结肠或脓毒症休克。由于CD检测条件受限,我国尚未将其纳入医院感染重点监测目标,这在一定程度上影响了疾病后续的诊治。快速鉴别艰难梭菌感染(Clostridioides difficile infection, CDI)及高产毒株对早期临床诊断和精准治疗至关重要。
目前,CD鉴定主要基于病原学检测、毒素检测、基因检测等方法。国际金标准(产毒培养或细胞培养中和试验)因操作复杂未常规应用于临床。毒素A/B酶免疫分析(EIAs)特异度高但灵敏度受标本限制,超灵敏毒素检测技术尚未普及。谷氨酸脱氢酶(GDH)检测虽快速灵敏,因无法区分产毒/非产毒株,仅作初筛。核酸扩增检测(NAAT)(如PCR/qPCR)兼具良好的灵敏度和特异度,但高成本制约了其临床推广。因此,开发兼具快速、高灵敏度/特异度及低成本的毒素基因检测技术对优化CDI诊疗体系具有重大意义。
基于艰难梭菌tcdC基因的新型LAMP检测方法的研发及临床诊断效能评估
作者:肖园园1,段菊屏2,周景翔1,黄琴3,卿琰3,王海波3,吴安华1,4,5,李春辉1,4,5
单位:1. 中南大学湘雅医院医院感染控制中心;2. 湖南中医药大学附属长沙市中医医院;3. 湖南大学分子诊断与分子影像联合实验室;4. 中南大学湘雅医院超级耐药菌感染防治研究中心;5. 国家老年疾病临床研究中心(湘雅医院)
摘 要
目的 研发一项快速鉴定艰难梭菌并能明确高产毒株的检测方法,开展临床评估。
方法 利用环介导等温扩增(LAMP)法,基于tcdC、tcdA、tcdB基因来鉴定艰难梭菌,并评估该检测技术的灵敏度、特异度和总体一致性。
结果 共完成499例疑似艰难梭菌感染腹泻住院患者粪便标本检测,艰难梭菌检出率为12.8%(64/499),其中产毒艰难梭菌的检出率为10.8%(54/499)。本检测方法针对tcdA的灵敏度为87.2%,特异度为98.9%,阳性预测值为89.1%,阴性预测值为98.6%;对tcdB的灵敏度为88.2%,特异度为99.6%,阳性预测值为90.0%,阴性预测值为98.7%。不同菌株总毒素量各有不同,但A+B+菌株平均产毒量(1.79μg/mL)高于A-B+菌株(0.72μg/mL)和A-B-菌株(<0.10 μg/mL)。
结论 本便携式高通量LAMP检测方法能快速、高效鉴定艰难梭菌并且明确高毒株。






引文格式
肖园园,段菊屏,周景翔,等.基于艰难梭菌tcdC基因的新型LAMP检测方法的研发及临床诊断效能评估[J]. 中国感染控制杂志,2025,24(4):451-459. DOI:10.12138/j. issn.1671-9638.20255458.
XIAO Yuanyuan, DUAN Juping, ZHOU Jingxiang, et al. Development and clinical diagnostic efficacy of a novel LAMP method targeting the tcdC gene in Clostridioides difficile[J]. Chin J Infect Control, 2025,24(4):451-459. DOI:10.12138/j. issn.1671-9638.20255458.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#艰难梭菌# #tcdC#
14