Genome Med:多学科协作推进罕见病全基因组测序临床应用
2025-07-14 熊佳仪 MedSci原创 发表于上海
研究成功展示了GS联合多学科团队诊疗的临床价值,为未来罕见病的基因诊断和管理奠定了坚实基础。
罕见病患者面临诊断延迟、治疗手段有限和个性化遗传咨询不足等问题。传统检测手段如全外显子组测序(ES)和染色体芯片(CMA)虽能诊断许多病例,但对非编码区变异及结构变异(SV)识别能力有限。全基因组测序覆盖范围全面,能精准捕获单核苷酸变异(SNV)、小插入缺失(INDEL)、复杂结构变异及线粒体基因变异等,报道诊断率最高可达70%。在此背景下,如何于临床环境开展GS并有效转化为诊疗决策,是精准医疗的重要挑战。
该前瞻性、多中心、多学科协作的观察性队列研究,由韩国多家三甲医院及基因检测企业联合发起,于2023年8月至11月间开展,共纳入901名参与者,其中包括387位疑似罕见病患者(系谱中照顾主要个体,称为proband)及514名其家属。研究旨在评估基于全基因组测序技术的诊断效能、解读复杂变异的能力及临床意义,并辅以系统化、多学科遗传咨询支持,实现精准医疗在真实世界的落地。最终结果发表在Genome Medicine期刊上。
本研究涵盖遗传医学医生、实验室技术人员、遗传咨询师等多专业团队,结合电子问卷采集患者及家庭遗传信息。GS采用标准化流程,从DNA提取、测序、数据分析至解读均纳入严谨质控。诊断结果分为“诊断性”“不确定”和“阴性”三类,结合临床表现及既往检测结果综合判断,并对高影响遗传变异给予深度遗传咨询辅导。
研究结果
1. 人群基本特征及家系构成
疾病类别涵盖神经发育障碍(25.3%)、眼科疾病(13.7%)、形态异常综合征(11.1%)等多方面。
2. 诊断率和遗传变异类型
- 诊断性结果获得率为27%(104/387,95%CI:22.5%-31.3%),不确定结果占9%(35/387)。
- 诊断携带的变异类型中,单核苷酸变异及小型INDEL占77.9%,结构变异占21.2%,包括14例拷贝数变异及其他复杂SV。
- 约40.7%病理变异为新变异,37.3%为新发变异。
- 11.5%(16/139家系)的关键诊断性变异仅通过GS识别,包括罕见深部内含子变异、线粒体变异及小型CNV等。
3. 影响因素分析
- 儿童患者诊断率高于成人(30.6% vs. 21.5%,p=0.048)。
- 家系深度增强,诊断率显著提升:单一proband检测诊断率15.8%,三代家系29.5%,四代家系最高70%。
- 既往进行过遗传检测的患者诊断率显著更高(34.9% vs. 20.3%,p=0.013)。
4. 诊断率按疾病类别分布
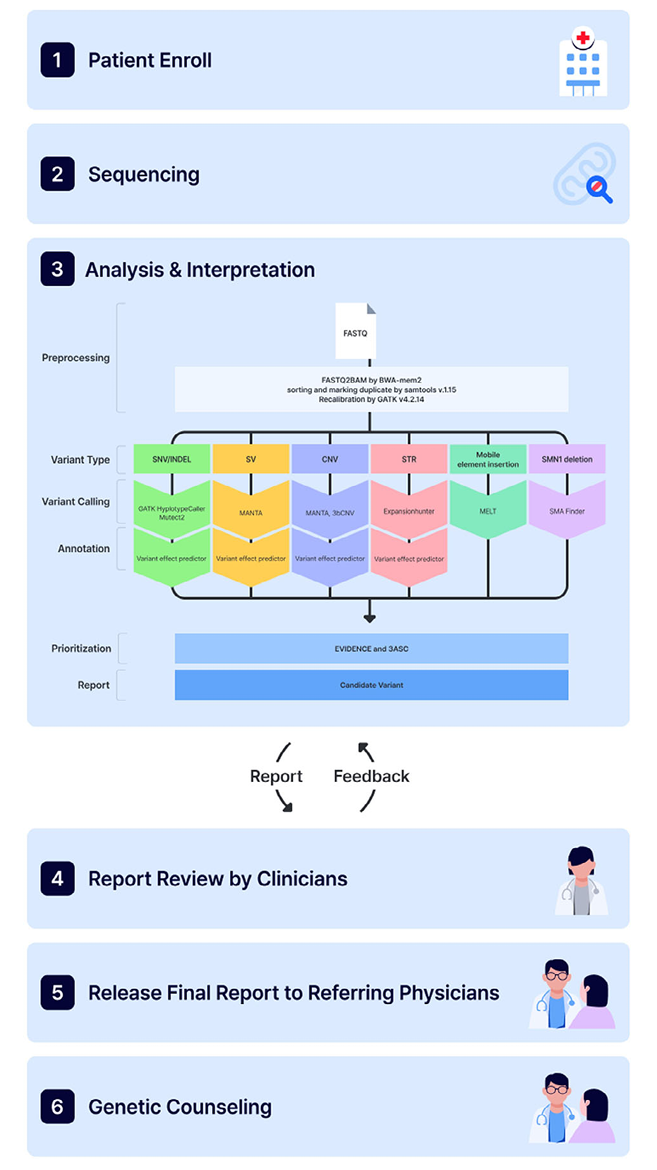
图 诊断流程示意图
5. 次生发现与患者意愿调查
- 94.7%患者及家属表达希望获知次生遗传信息,尤其关注可治疗性、遗传风险及疾病严重程度。
- 次生发现中4.7%家系携带15种已知致病基因的病理变异,最多见PCSK9及BRCA2基因变异。
- 信息披露引发的担忧中,以疾病风险认知、隐私及情绪反应为主。
6. 临床干预与遗传咨询效益
- 基于GS诊断结果,38.8%家系开展了相关临床管理,包括疾病监控、靶向治疗及器官移植等。
- 86名接受深度遗传咨询者中,心理赋能显著提升(由88.6升至92.1,p<0.007)。
- 咨询满意度高,超过一半表示遗传咨询促进了决策及疾病理解。
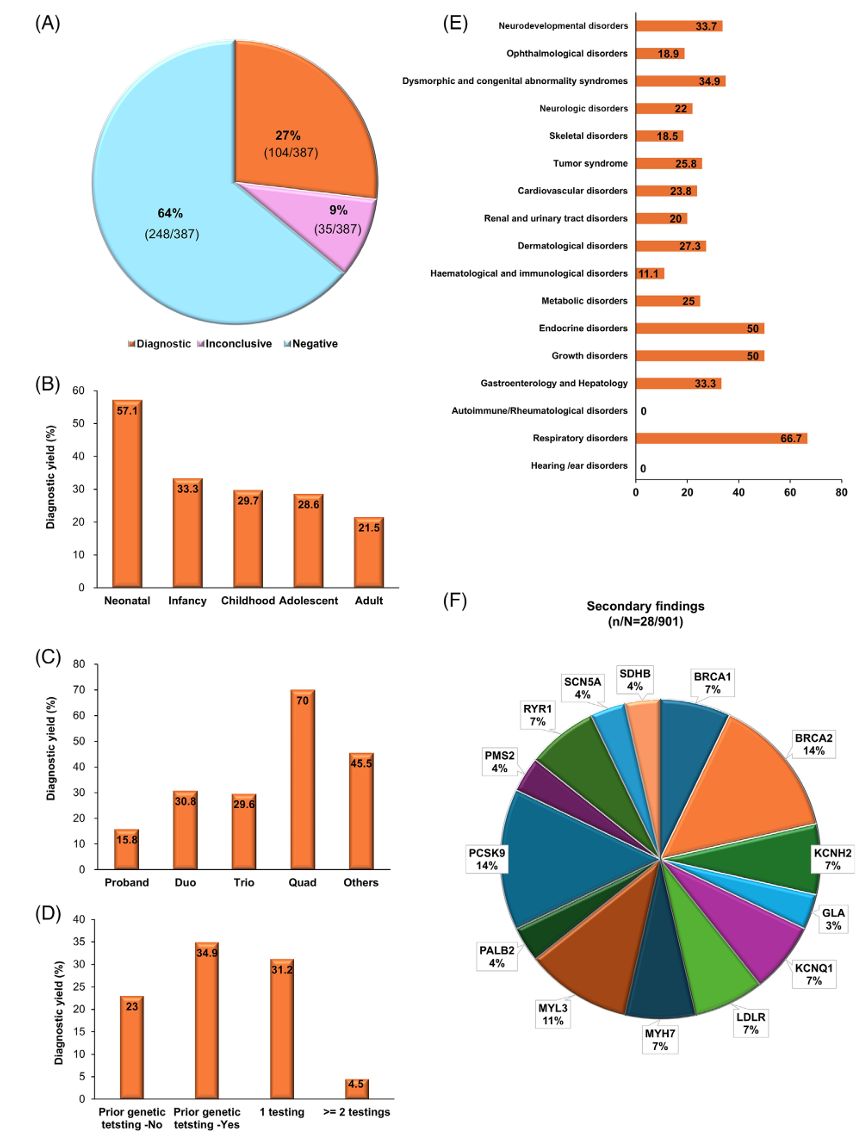
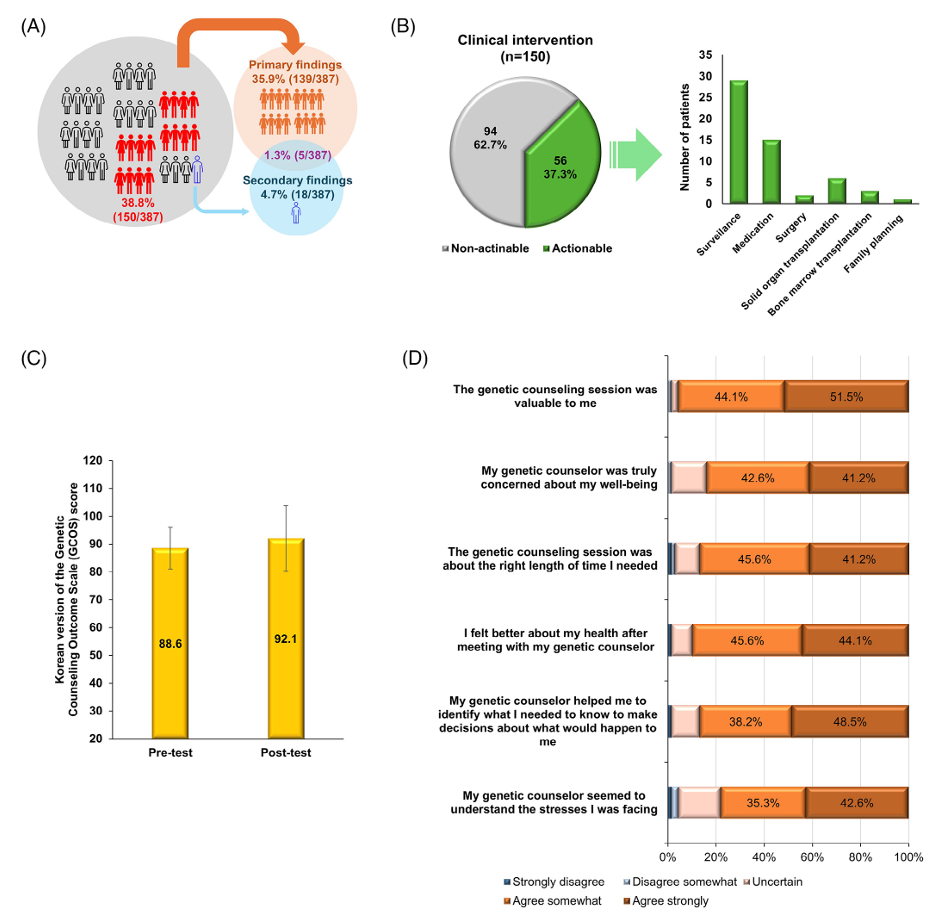
图:诊断率及咨询满意度
研究价值与意义
本研究首创性地通过多中心协作、系统化流程将全基因组测序技术规范应用于罕见病的临床诊断,显著提升了诊断率及复杂变异识别能力。这为罕见病患者提供了更为全面而精准的遗传学解释,促进早期诊断和个体化治疗策略的落地。研究强调了家系信息完整性的重要性,建议扩大亲属采样来优化诊断效果。
此外,研究还强调遗传咨询作为GS流程不可或缺的环节,帮助患者及家属充分理解检测结果、缓解焦虑情绪并支持后续决策,体现精准医疗的人文关怀。患者高度关注次生发现信息,提示临床实践中需建立合理的信息披露机制,兼顾知情权与心理承受能力。
不过,研究也认识到样本容量有限及随访时间较短的限制,特别是针对一些成人慢发性或多因素疾病的诊断,仍需更大规模、多中心的长期研究验证GS临床经效性及经济效益。
总体来说,研究成功展示了GS联合多学科团队诊疗的临床价值,为未来罕见病的基因诊断和管理奠定了坚实基础。
原始出处:
Hwang S, Seo GH, Choi IH, et al. Clinical implementation of a multidisciplinary pipeline for genome sequencing in rare diseases: A prospective, multicenter, observational cohort study. Genome Med. 2025; e70401. https://doi.org/10.1002/ctm2.70401
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言





















#全基因组测序# #罕见病#
10 举报