European Radiology:通过多模态深度学习进行胰腺癌的端到端预后评估
2025-06-12 shaosai MedSci原创 发表于上海
人工智能(AI)目前广泛应用于医学图像分析和癌症研究,在预测喉癌、乳腺癌、肾癌、结直肠癌和胰腺癌等多种癌症的患者预后方面显示出良好效果。
胰腺导管腺癌(PDAC)的五年生存率仅 5%,仍是全球致死率最高的恶性肿瘤之一,给患者、临床医生和研究人员带来巨大挑战。影像学在 PDAC 患者的分期适配治疗分层中至关重要,其中增强 CT(CECT)是主要的成像方式。癌症分期的临床标准是 TNM 系统,该系统考虑肿瘤范围(T)、区域淋巴结转移(N)和远处转移(M)。这一分期系统旨在将患者群体划分为不同生存亚组(IA、IB、IIA、IIB、III、IV 期),目前用于指导 PDAC 的治疗策略。仅 20% 的患者(I-III 期)符合根治性切除条件,因此手术切除联合辅助 / 新辅助治疗是他们获得长期生存或治愈的主要希望。超过 90% 接受根治性切除的 PDAC 患者会出现局部复发、远处复发或转移。此外,相同 TNM 分期的患者总生存率差异显著。这种变异性反映在 TNM 分期的预后效能上,可通过一致性指数(c-index)量化 —— 该指标衡量模型对不同生存结局患者的区分能力。c-index 为 0.5 表示区分能力与随机无异,1 则代表完美的预后准确性。据报道,可切除和不可切除患者的 TNM 分期 c-index 分别低至 0.57 和 0.611。显然,TNM 分期缺乏预后准确性,与总生存率无显著相关性,且在指导治疗决策时不可靠。
鉴于传统 TNM 分期的局限性,迫切需要更优的 PDAC 分层系统。人工智能(AI)目前广泛应用于医学图像分析和癌症研究,在预测喉癌、乳腺癌、肾癌、结直肠癌和胰腺癌等多种癌症的患者预后方面显示出良好效果。尽管临床医生通常使用多种数据来源指导决策(例如,将放射影像与临床或实验室结果及组织病理学评估结合,若可用),但绝大多数基于影像的 PDAC 预后 AI 研究仅依赖单一数据类型。多模态 AI 算法可从多种数据来源和类型中提取并整合信息,以做出更全面的决策,模拟临床医生目前用于解决癌症预后等复杂临床问题的输入条件。

最近,发表在European Radiology 上的一篇文章探究了人工智能(AI)如何通过整合多源数据提升胰腺癌预后准确性。
研究纳入荷兰中心(2004-2023 年)经组织病理学和 / 或影像 / 随访证实的胰腺导管腺癌(PDAC)患者作为开发队列,另选取荷兰和西班牙中心的两个 PDAC 队列用于外部验证。构建包含临床变量、增强 CT 影像及两者结合的预后模型,以预测高风险短期生存。所有模型采用五折交叉验证训练,并通过时间依赖性受试者工作特征曲线下面积(AUC)评估。
开发队列包含 401 例患者(203 例女性,198 例男性,中位总生存期(OS)347 天,IQR:171-585),其中 98 例(24.4%)为短期生存者(OS < 230 天),303 例(75.6%)为长期生存者。外部验证队列含 361 例患者(165 例女性,138 例男性,中位 OS 404 天,IQR:173-736),110 例(30.5%)短期生存者和 251 例(69.5%)长期生存者。内部验证中,多模态模型预测短期与长期生存的 AUC 最佳(0.637,95% CI:0.500-0.774),外部验证 AUC 分别为 0.571(95% CI:0.453-0.689)和 0.675(95% CI:0.593-0.757)。
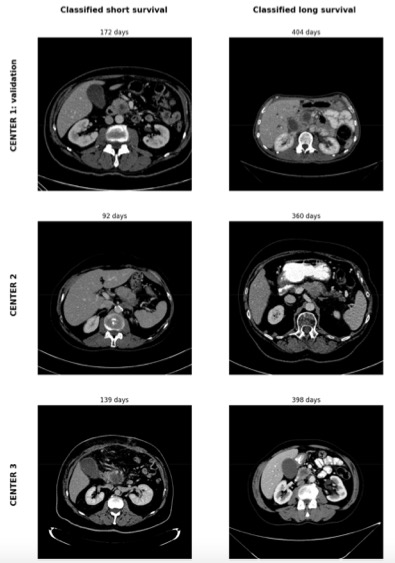
图 在“CENTER 1:验证集”、“CENTER 2”以及“CENTER 3”中所确定的短期存活者和长期存活者的患者实例
研究表明,多模态 AI 可预测 PDAC 患者的长短期生存,有望成为临床决策中的预后评估工具。
原文出处:
Megan Schuurmans,Anindo Saha,Natália Alves,et al.End-to-end prognostication in pancreatic cancer by multimodal deep learning: a retrospective, multicenter study.DOI:10.1007/s00330-025-11694-y
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#胰腺癌#
23 举报