读书报告 |多维推荐系统鉴定结直肠癌肝转移治疗靶点
2025-07-18 iCombo iCombo 发表于上海
本研究验证的候选靶点具有转化医学潜力,有望填补当前CRLM诊疗中的空白。研究强调多维度数据融合在癌症精准医疗中的价值,为未来开发基于AI的肿瘤决策系统提供了新思路。
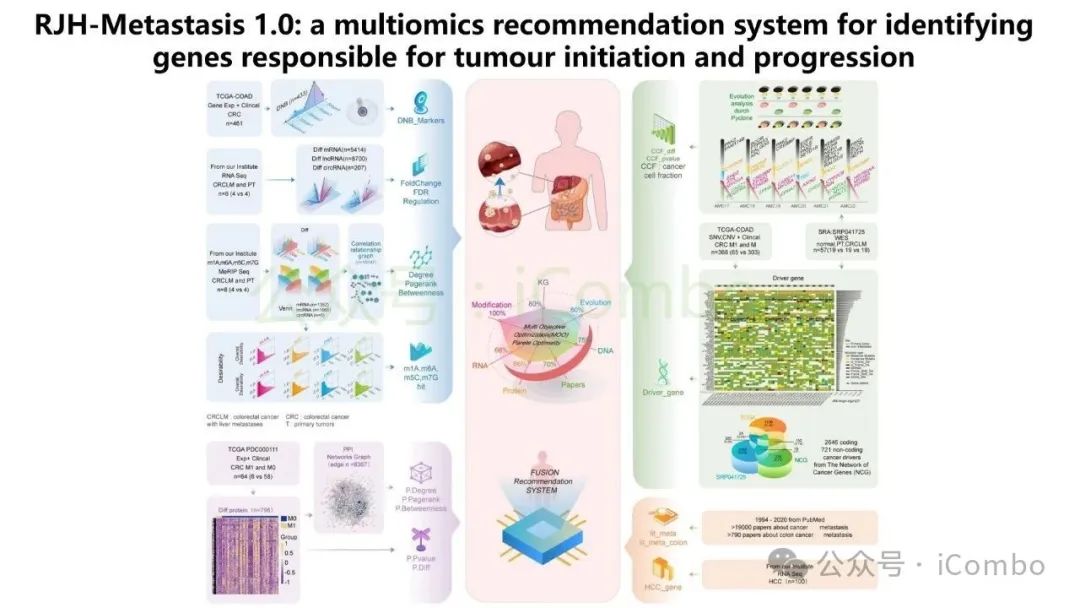
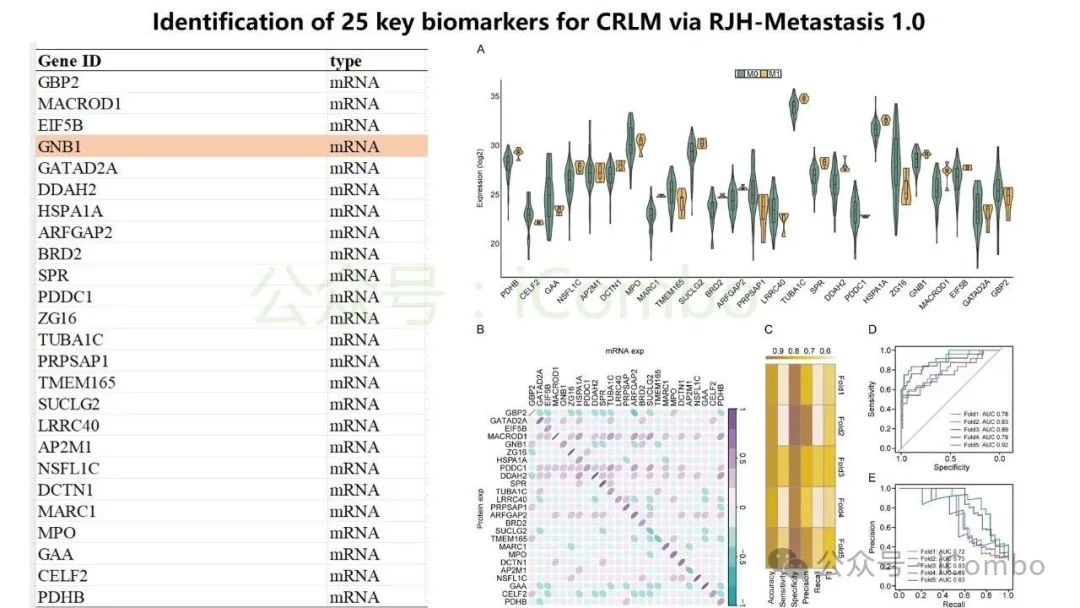
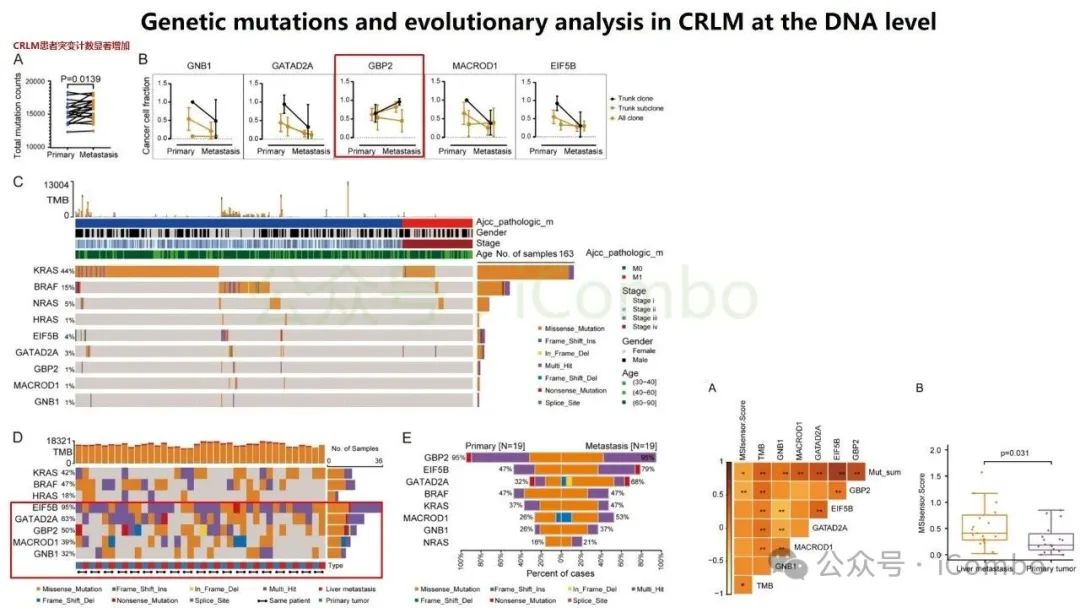
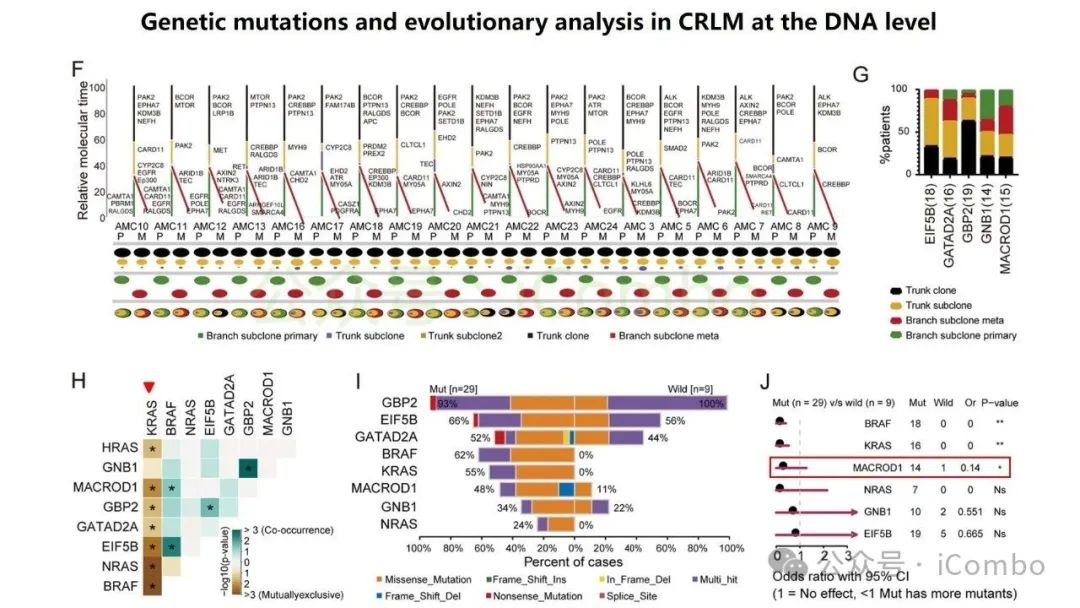
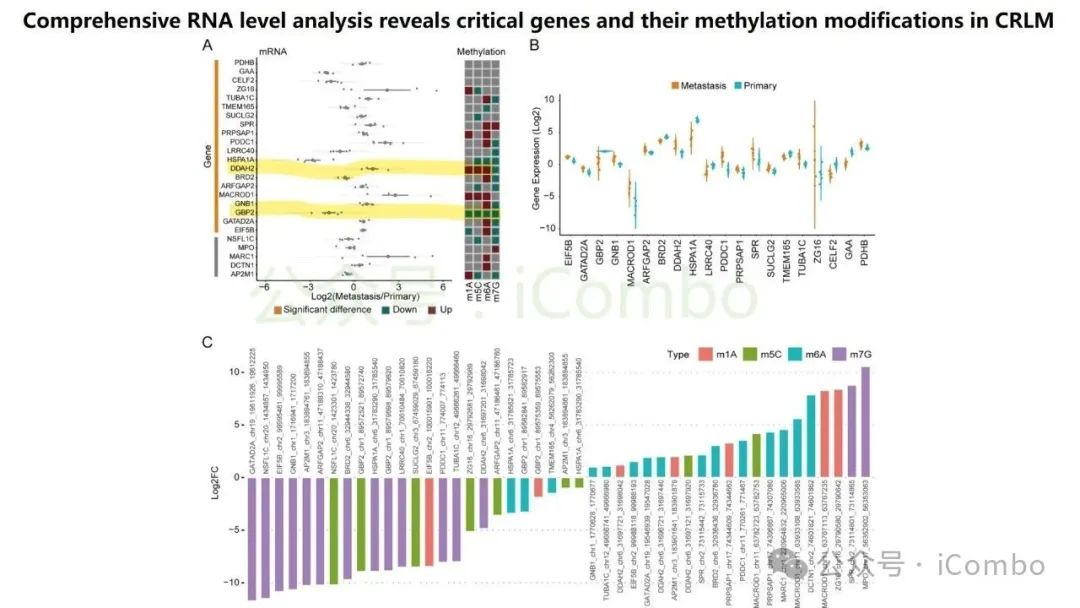
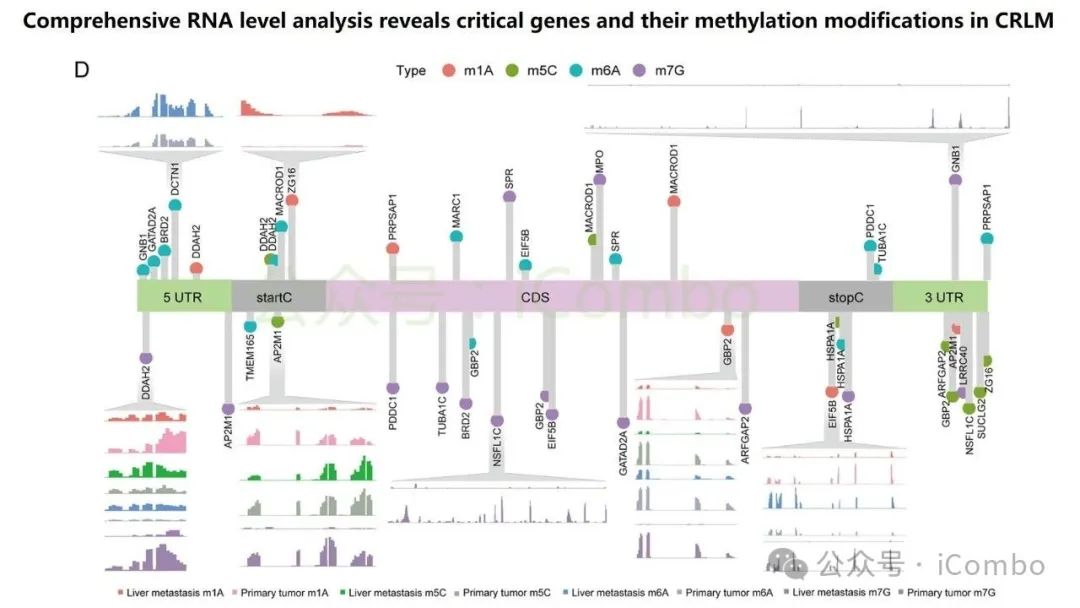
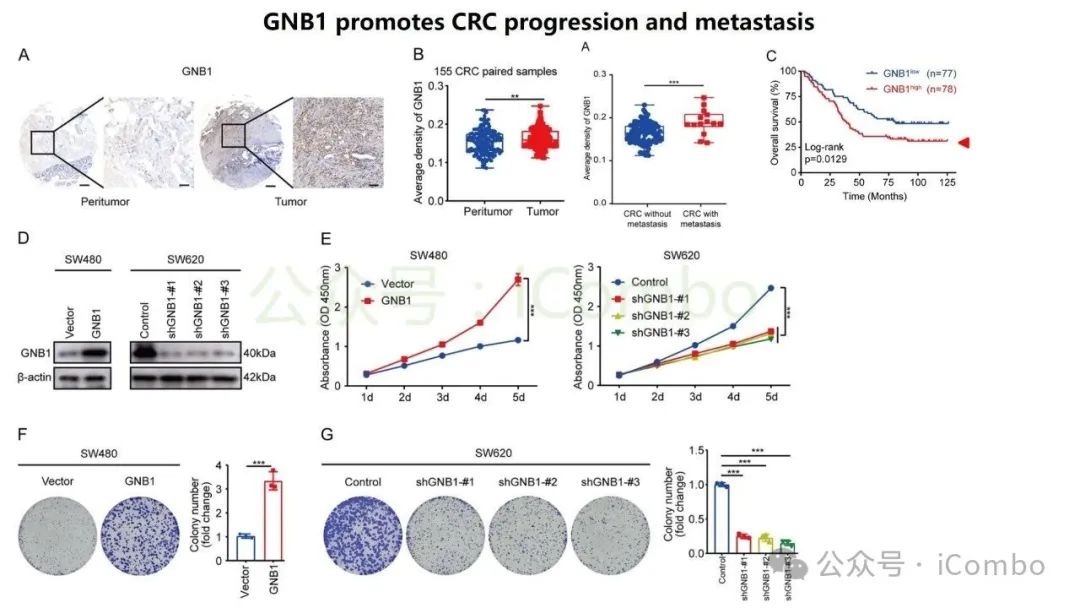
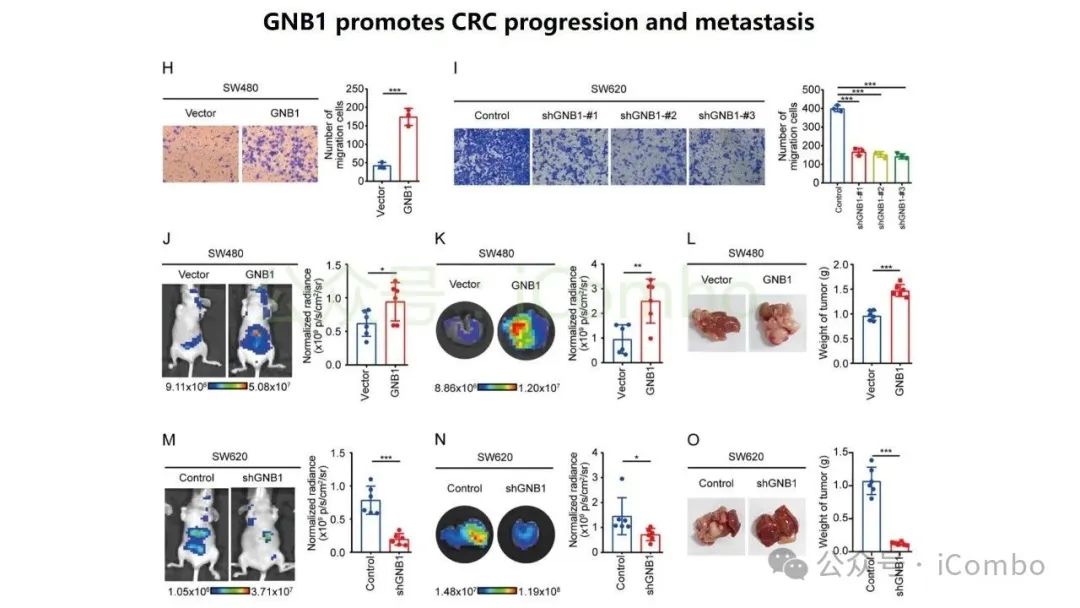
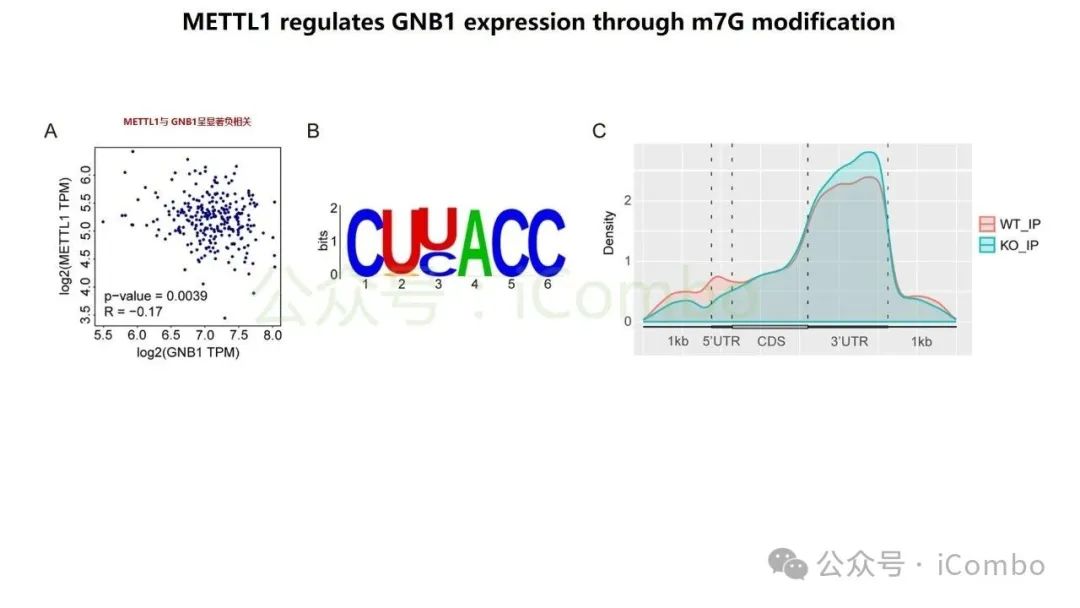
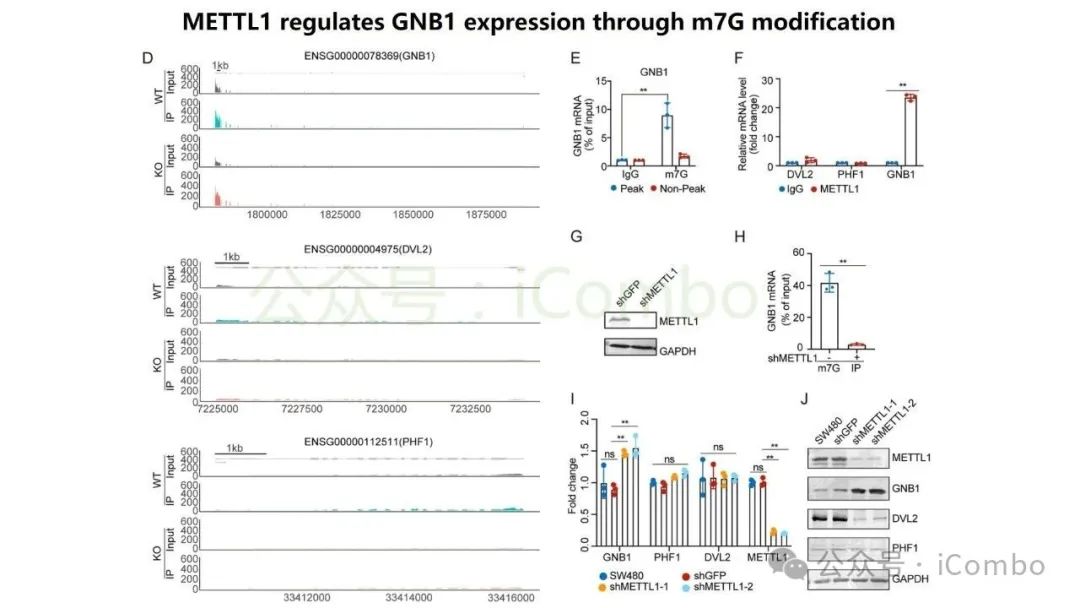
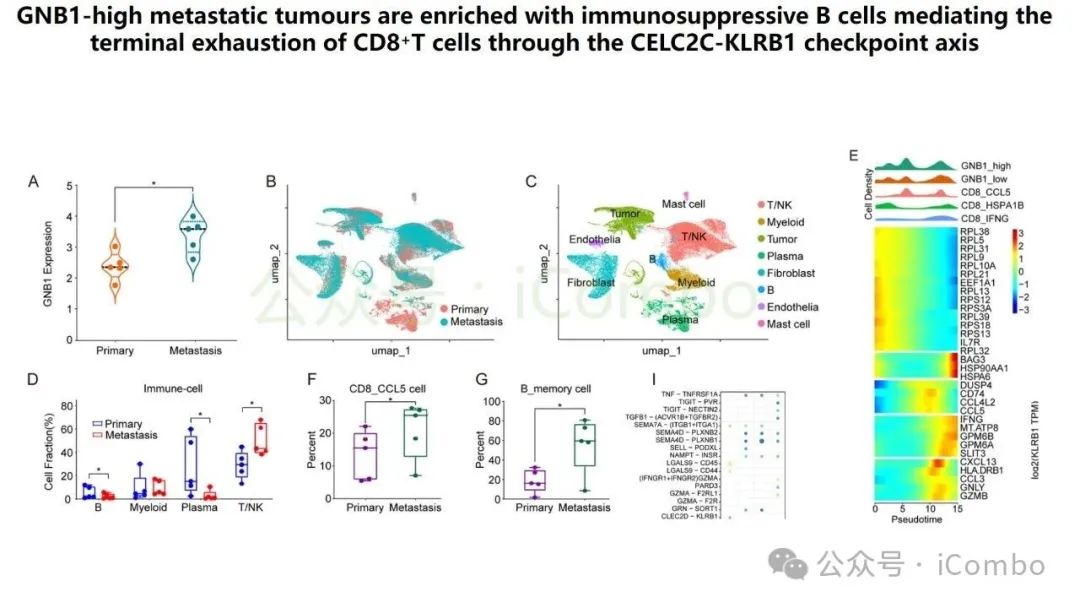
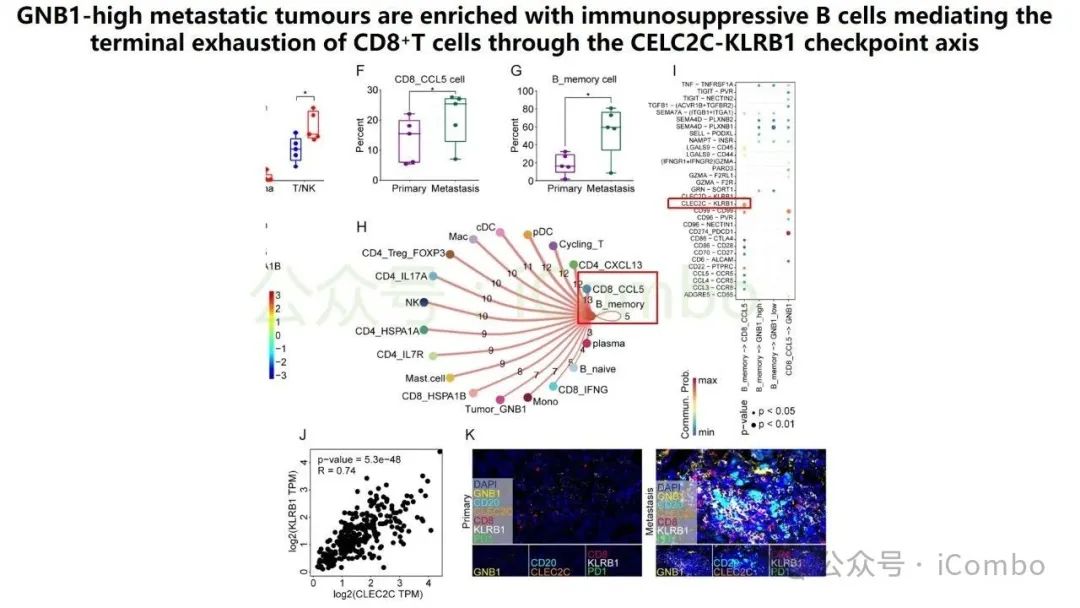
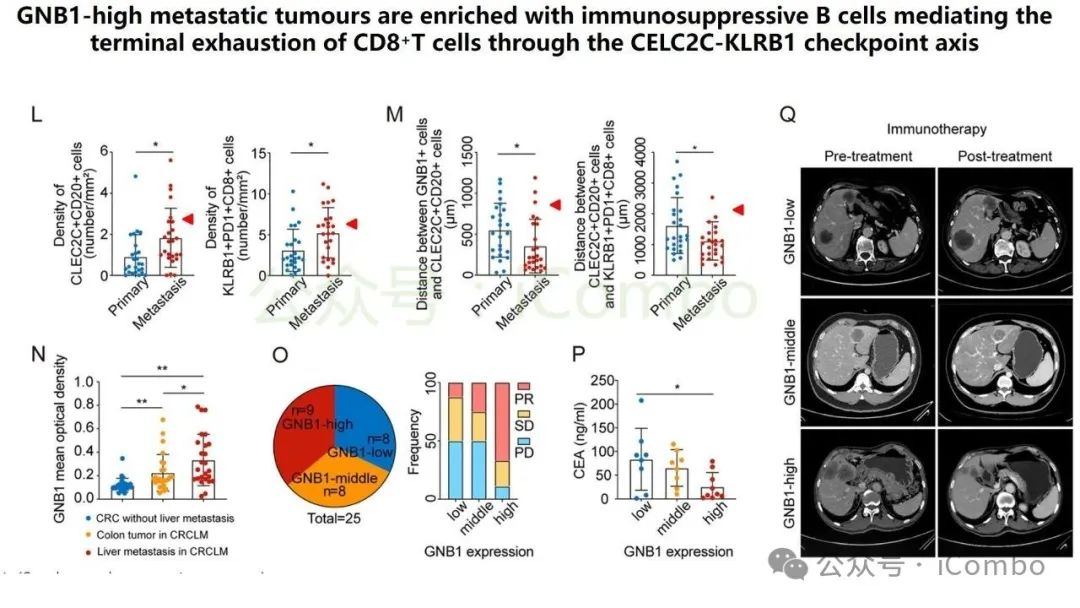
导读 结直肠癌肝转移(CRLM)是CRC患者死亡的主要原因。尽管近年来随着治疗策略的发展CRC生存率有所提高,但CRLM患者的预后仍然不容乐观。但其分子机制复杂,且现有单组学分析方法难以全面揭示其生物学特征,无法完全阐明肿瘤分子谱的复杂性,很有可能会忽视关键的分子靶点。基于组学的临床发现目前是癌症研究中使用的一种常见策略,用于了解复杂的肿瘤分子谱,并识别在癌症的发展、进展和治疗中发挥关键作用的分子。迄今为止,大多数研究主要依赖于单组学分析方法,这些方法侧重于癌症的特定生物层,但这一固有特征突出了这些方法在解决表征肿瘤的复杂相互作用网络方面的局限性。尽管单一组学分析提供了有价值的见解,但它们无法捕捉到肿瘤发展和进展过程中存在的全面分子特征,也可能无法确定具有治疗价值的靶点。因此,一种新的综合多组学方法将使我们能够更全面地了解肿瘤生物学,为靶向治疗的发展奠定更坚实的基础。本研究旨在开发一个多维推荐系统(RJH-Metastasis 1.0),通过整合基因组、转录组、蛋白质组和文献证据等多组学数据,识别CRLM的关键生物标志物和治疗靶点,以弥补传统单组学分析的局限性。其构建的RJH-Metastasis 1.0系统整合了43个特征参数,覆盖DNA突变、RNA表达与修饰、蛋白质互作及文献支持等多个维度,再通过多目标优化策略,筛选出了25个与CRLM显著相关的基因,其中GNB1、GATAD2A、GBP2、MACROD1和EIF5B被进一步验证为关键基因。研究发现,GNB1在CRLM中表现出独特的调控模式:其DNA突变频率较低,但RNA转录和蛋白质表达显著上调。机制研究表明,GNB1的表达受METTL1介导的m7G RNA修饰调控,METTL1敲低会减少GNB1 3'UTR区域的m7G修饰,从而促进其翻译。此外,GNB1通过促进记忆B细胞与CD8+ T细胞间的CLEC2C-KLRB1免疫检查点互作,形成免疫抑制微环境,进而影响PD-1抗体治疗的疗效。临床分析显示,GNB1高表达患者对免疫治疗的响应更佳,提示其作为潜在生物标志物的价值。本研究利用机器学习算法和网络分析,系统筛选了与肝转移进展相关的关键生物标志物、信号通路及潜在药物靶点,尤其关注肿瘤微环境与分子异质性的影响。该框架不仅提升了CRLM分子分型的准确性,还为个体化治疗策略的制定提供了数据支持。本研究验证的候选靶点具有转化医学潜力,有望填补当前CRLM诊疗中的空白。研究强调多维度数据融合在癌症精准医疗中的价值,为未来开发基于AI的肿瘤决策系统提供了新思路。(Mol Cancer. 2024 Oct 24;23(1):239.doi: 10.1186/s12943-024-02155-z)



本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#结直肠癌肝转移# #治疗靶点#
5 举报