NEJM:长效肽 - 抗体偶联物 MariTide 每月给药,实现肥胖患者 52 周减重超12%
2025-06-25 MedSci原创 MedSci原创 发表于上海
肥胖治疗药物的发展正走向更以患者便利性和依从性为核心的长效方案设计。MariTide这一创新长效GLP-1/GIP双机制联合疗法用抗体偶联大幅延长药物半衰期,成功实现了多达一个月甚至更低频率给药,
肥胖作为全球范围内高发的慢性疾病,严重威胁公共健康并增加多种代谢和心血管疾病的风险。当前针对肥胖的药物治疗主要依赖GLP-1受体激动剂(如司美格鲁肽)及其联合疗法,虽取得显著体重和血糖控制效果,但用药频率较高(多为每周),长期依从性受限。此外,肥胖合并2型糖尿病患者的体重下降幅度通常低于单纯肥胖患者,亟需创新疗法满足临床需求。
Maridebart Cafraglutide(MariTide)是一种创新型长效肽-抗体偶联物,结合GLP-1受体激动与GIP受体拮抗双重机制,理论上可实现更强的体重与代谢调控,其抗GIP受体单抗载体赋予药物约21天的血浆半衰期,显著超越现有GLP-1疗法,使得每月或更低频次给药成为可能。同时,前期Ⅰ期研究显示良好的安全与耐受性。
近日,《新英格兰医学杂志》(NEJM)发表了一项关于MariTide治疗肥胖的多中心、随机、双盲、安慰剂对照的Ⅱ期临床试验结果。该试验涵盖465名单纯肥胖患者及127名合并2型糖尿病的肥胖患者,探讨了不同剂量与给药频率下马瑞得巴特的疗效、安全性及耐受性。结果表明,每月给药方案可实现肥胖患者52周减重12%以上,伴血糖指标、心血管危险因素等多项代谢参数改善,且通过剂量逐步递增优化了胃肠道副反应。此项研究意义重大,标志着肥胖治疗策略向更长效、易依从药物转变,具有广泛的临床应用前景。

研究设计与方法
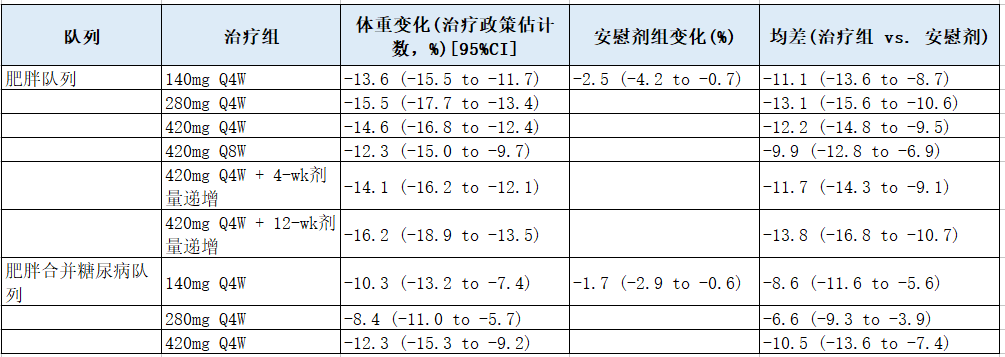
本研究为多国开展的Ⅱ期随机双盲安慰剂对照试验,设两个研究队列:(1)肥胖患者队列(BMI≥30或≥27且伴至少一项合并症,无2型糖尿病);(2)肥胖伴2型糖尿病患者队列(BMI≥27,HbA1c 7-10%,口服降糖药稳定)。肥胖队列按照7个组别按3:3:3:2:2:2:3比例随机接受马瑞得巴特不同剂量/给药频率方案(140 mg、280 mg、420 mg每4周一次、420 mg每8周一次,以及420 mg每4周一次配4周或12周剂量递增方案)或安慰剂。肥胖合并糖尿病队列4组分配(140 mg、280 mg、420 mg每4周一次,无剂量递增)与安慰剂1:1:1:1随机分组。主要终点为52周时体重变化的百分比。次要终点涉及血糖控制、胰岛素水平、心血管代谢指标、体成分变化及安全性评估。
研究结果
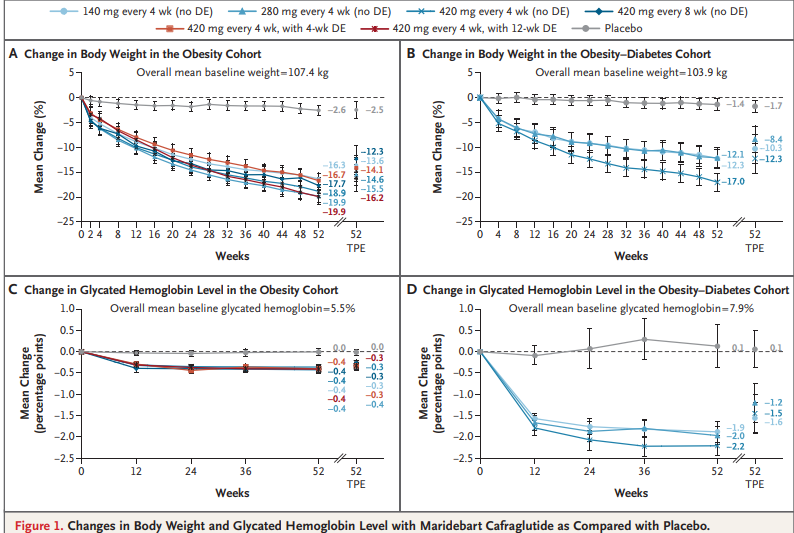
体重变化趋势显示,MariTide治疗组体重持续下降,52周未见减重平台期形成,提示疗效有望进一步积累。合并2型糖尿病患者的平均HbA1c下降1.2%-1.6%,安慰剂组基本无变动。
体成分分析示脂肪质量大幅减少,瘦体质量减少较少,符合健康减重预期。血压、Hs-CRP及部分血脂均有改善,呈现心血管风险降低趋势。
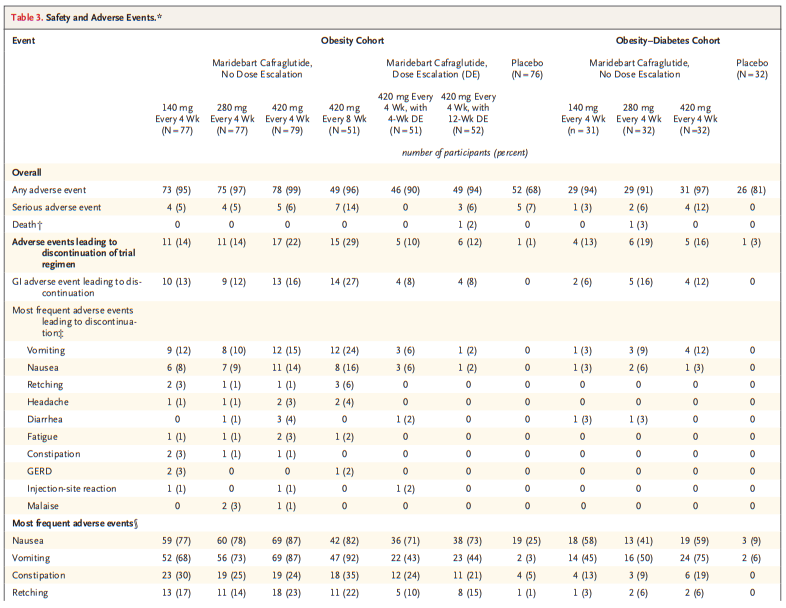
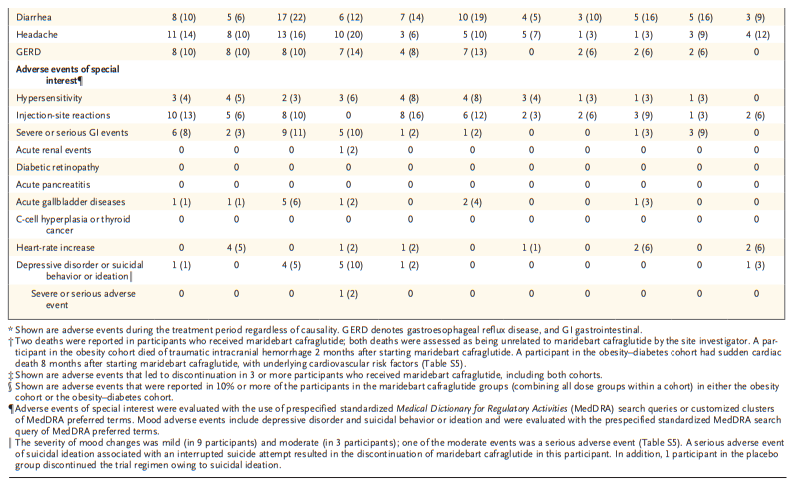
安全性方面,治疗组胃肠道不良事件常见(恶心、呕吐等),但多为轻中度,剂量递增或低起始剂量方案有效减少相关不适及治疗中断。总体严重不良事件和死亡率低,未发现新安全信号及胰腺炎、糖尿病视网膜病变等严重并发症。
研究价值与意义
本研究首次报道一种结合GLP-1受体激动和GIP受体拮抗双重机制的长效月度用药——MariTide产生大幅度和持续性的减重效果,兼具良好血糖控制作用,其独特的抗体偶联长半衰期设计,突破了现有肥胖药物亟需频繁给药的瓶颈,为患者带来了更低治疗负担、更高依从性可能。尤其是在肥胖合并2型糖尿病患者中,取得同步且安全的体重及血糖改善,显示出极具临床转换潜力。
此外,剂量递增策略明显降低了常见的胃肠道副作用,提高了耐受性和治疗持续性,为未来临床推广提供了重要实践依据。值得一提的是,研究证明了GIP受体拮抗虽与GIP受体激动作用于体重控制均有效,但机制理论仍需进一步探索,未来相关机制研究与药物优化潜力巨大。
随着Ⅱ期后续维持期研究开展以及Ⅲ期大型注册试验启动,MariTide有望成为肥胖领域一款突破性长效新药,满足临床对高效、低频、良好耐受肥胖治疗的市场需求,对改善全球肥胖相关疾病负担具有重要推动作用。
梅斯小编点评
肥胖治疗药物的发展正走向更以患者便利性和依从性为核心的长效方案设计。MariTide这一创新长效GLP-1/GIP双机制联合疗法用抗体偶联大幅延长药物半衰期,成功实现了多达一个月甚至更低频率给药,且在降重和降糖效果上表现优异,堪称肥胖治疗新里程碑。在实际临床操作中,降低胃肠道副作用及提高耐受性的剂量递增设计尤为关键,为后续大型临床试验和临床推广奠定基础。
未来研究可进一步探究GIP受体拮抗与激动机理差异,优化个性化用药方案,以及评估更长远的心血管及代谢终点效应。此外,比较不同肥胖药物的疗效、安全和依从性,结合真实世界研究数据,将为临床合理用药提供重要指导。
原始出处:
Jastreboff AM, Ryan DH, Bays HE, et al. Once-Monthly Maridebart Cafraglutide for the Treatment of Obesity — A Phase 2 Trial. N Engl J Med. Published June 23, 2025; DOI: 10.1056/NEJMoa2504214.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言





















#肥胖# #MariTide#
23 举报