连发两篇《柳叶刀》!无进展生存期近乎翻倍,或改变肝癌临床治疗实践
2025-01-11 医学新视点 医学新视点 发表于陕西省
基于这两项研究结果,临床可考虑在疾病早期阶段采用免疫检查点抑制剂联合用药的策略,因为相比于现在的疾病晚期用药策略,早期用药可能可以在患者身体和心理负担都较低时,更好地控制肿瘤。
肝癌早期临床症状不典型,常见的有乏力、上腹部疼痛、食欲缺乏、恶心呕吐等,容易被忽视,因此多数患者在就诊时已处于疾病晚期,无法行根治性手术切除。目前,针对中晚期肝癌的治疗主要有放射治疗、消融治疗、经动脉化疗栓塞(TACE)、系统性抗肿瘤治疗等,临床医生会根据患者疾病不同分期选择不同的一线治疗措施。
TACE是可接受栓塞的不可切除肝癌患者的标准治疗方式,但中位无进展生存期(PFS)大约为7个月。基于免疫检查点抑制剂的免疫治疗改变了晚期肝癌的治疗局面,是当前系统性治疗的一线标准策略。因此,采用基于免疫检查点抑制剂与TACE的联合治疗方法,是值得临床持续探索的研究方向。
近日,《柳叶刀》连发两篇探索TACE联合免疫检查点抑制剂(PD-1抑制剂/PD-L1抑制剂)和血管内皮生长因子(VEGF)或多激酶抑制剂治疗肝癌的研究。其中EMERALD-1研究表明,相比于使用TACE+安慰剂的患者,采用TACE+度伐利尤单抗+贝伐珠单抗方案的患者,无进展生存期可达15个月,疾病进展和死亡风险降低了23%。LEAP-012研究也获得了相似的结果,相比于使用TACE+双联安慰剂的患者,采用TACE+帕博利珠单抗+仑伐替尼方案的患者,无进展生存期为14.6个月,疾病进展和死亡风险降低了34%;24个月总生存率为75%,死亡风险降低了20%。
《柳叶刀》发表的同期社论指出,这两项研究结果可能改变当前的临床实践,未来基于免疫检查点抑制剂的联合全身治疗,可能将成为适合TACE治疗的肝癌患者的治疗选择之一。
研究简介
EMERALD-1研究是一项随机、双盲、3期试验,纳入了616例接受TACE治疗的不可切除肝细胞癌患者,所有患者中位年龄65岁,其中78%为男性,22%为女性。研究人员将患者以1:1:1的比例随机分配入组,分别接受以下治疗:
-
TACE+度伐利尤单抗+贝伐珠单抗组(204例):TACE+度伐利尤单抗(1500 mg,每4周一次),而后同时接受度伐利尤单抗(1120 mg,每3周一次)+贝伐珠单抗(15 mg/kg,每3周一次);
-
TACE+度伐利尤单抗+安慰剂组(207例):TACE+度伐利尤单抗(1500 mg,每4周一次),而后接受度伐利尤单抗(1120 mg,每3周一次)+贝伐珠单抗的替代安慰剂(无菌盐水,每3周一次);
-
TACE+安慰剂组(205例):TACE+度伐利尤单抗的替代安慰剂(生理盐水,每4周一次),而后接受度伐利尤单抗的替代安慰剂(每3周一次)和贝伐珠单抗的替代安慰剂(每3周一次)。
研究结果显示,截至2023年9月11日,针对PFS的中位随访时间为27.9个月时,TACE+度伐利尤单抗+贝伐珠单抗组PFS为15.0个月(95%CI:11.1~18.9),显著长于TACE+度伐利尤单抗+安慰剂组的10.0个月(95%CI:9.0~12.7)和TACE+安慰剂组的8.2个月(95%CI:6.9~11.1)。
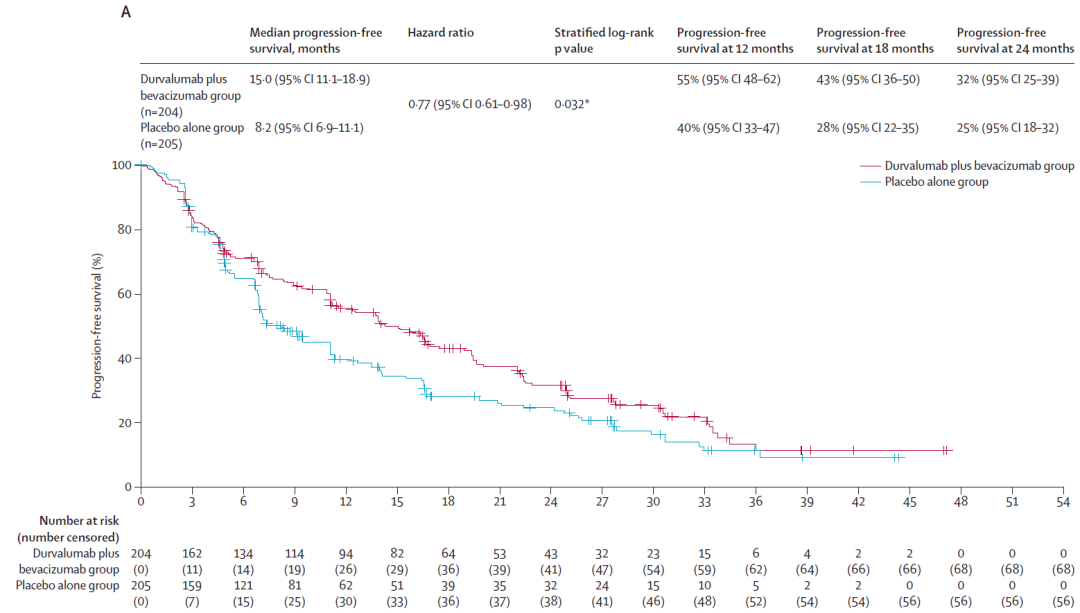

▲TACE+度伐利尤单抗+贝伐珠单抗组(红色)和TACE+安慰剂组(蓝色)(图A),TACE+度伐利尤单抗+安慰剂组(红色)和TACE+安慰剂组(蓝色)(图B)的PFS对比
相比于TACE+安慰剂组,TACE+度伐利尤单抗+贝伐珠单抗组疾病进展和死亡风险降低了23%(HR=0.77,95%CI:0.61~0.98,P=0.032);相比于TACE+安慰剂组,TACE+度伐利尤单抗+安慰剂组疾病进展和死亡风险降低了6%,但差异无统计学意义(HR=0.94,95%CI:0.75~1.19,P=0.64)。
安全性方面,常见的3~4级不良事件为高血压、贫血等,TACE+度伐利尤单抗+贝伐珠单抗组的患者,无一例因治疗相关不良事件死亡。
LEAP-012研究是一项随机、双盲、3期试验,纳入了全球33个国家480例Child-Pugh A级肝癌患者(即不适合治愈性治疗,但适合TACE)。研究人员以1:1的比例随机将患者分配接受TACE+仑伐替尼+帕博利珠单抗(237例)或TACE+双联安慰剂(243例)。所有患者中位年龄为66岁,其中83%为男性,17%为女性。
研究结果显示,截至2024年1月,中位随访时间为25.6个月。TACE+仑伐替尼+帕博利珠单抗组中位PFS为14.6个月(95%CI:12.6~16.7),显著长于TACE+双联安慰剂组的10个月。相比于TACE+双联安慰剂组,TACE+仑伐替尼+帕博利珠单抗组的疾病进展和死亡风险降低了34%(HR=0.66,95%CI:0.51~0.84,P=0.0002)。
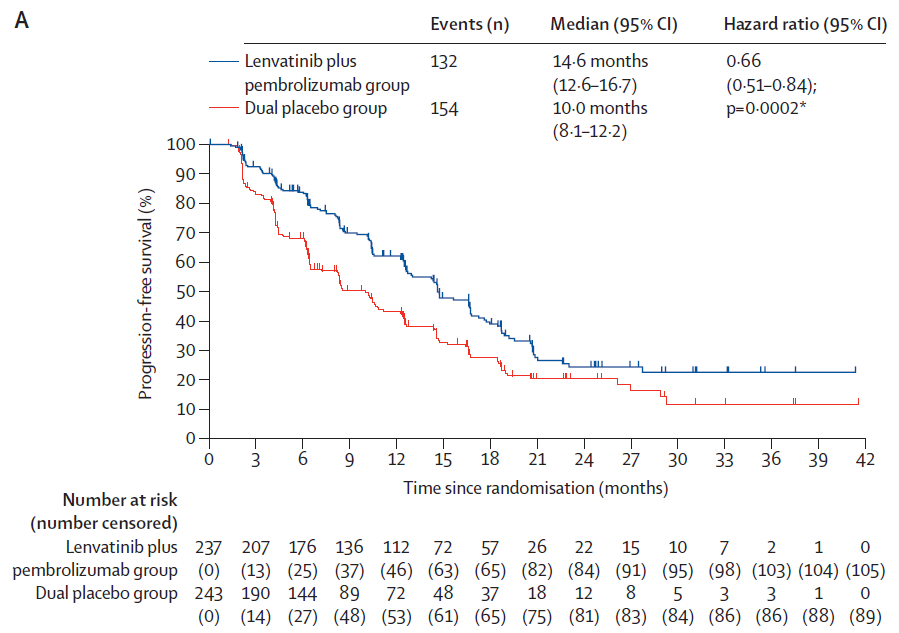
▲TACE+仑伐替尼+帕博利珠单抗组(蓝色)和TACE+双联安慰剂组(红色)中位PFS对比(图片来源:参考文献[1])
TACE+仑伐替尼+帕博利珠单抗组和TACE+双联安慰剂组分别有29%(69/237)和34%(82/243)的患者死亡,24个月总生存率分别为75%(95%CI:68~80)和69%(95%CI:62~74)。相比于TACE+双联安慰剂组,TACE+仑伐替尼+帕博利珠单抗组的死亡风险降低了20%(HR=0.80,95%CI:0.57~1.11,P=0.087)。
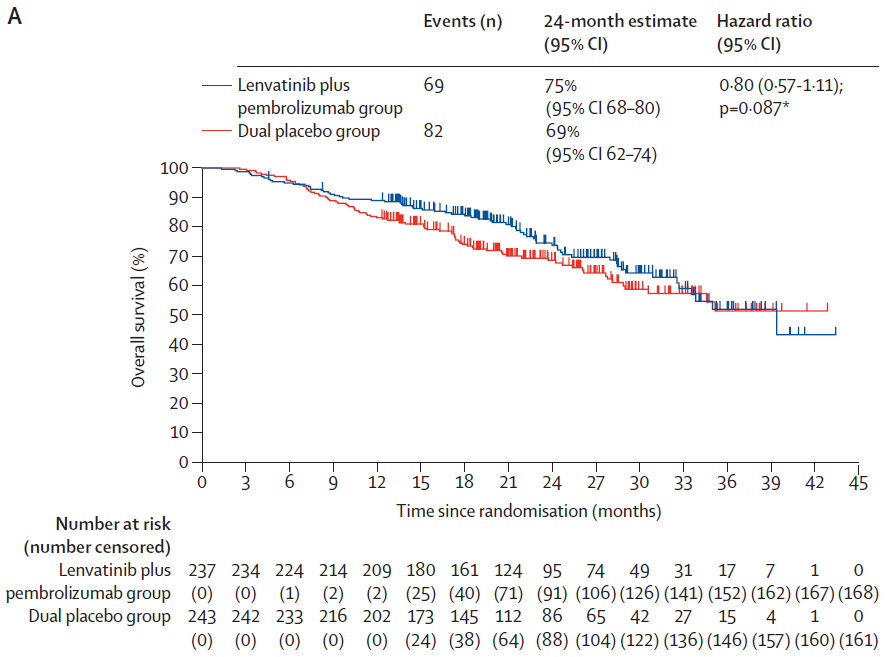
▲TACE+仑伐替尼+帕博利珠单抗组(蓝色)和TACE+双联安慰剂组(红色)24个月生存率对比(图片来源:参考文献[1])
安全性方面,TACE+仑伐替尼+帕博利珠单抗组和TACE+双联安慰剂组分别有71%和76%的患者发生3级及以上不良事件,以高血压、血小板计数降多见,且分别有4例和1例患者因治疗相关不良事件死亡。
研究解读
EMERALD-1研究和LEAP-012研究,均探索了免疫检查点抑制剂(度伐利尤单抗或帕博利珠单抗)与VEGF抑制剂(仑伐替尼或贝伐珠单抗)联合TACE的作用,且均采用经设盲独立中心审查的RECIST 1.1版评估的PFS作为主要研究结局,这是评估局部治疗(如TACE)的一种严格指标。不过,两个研究中患者开始系统性治疗的时间并不相同,LEAP-012研究中患者通常在首次TACE手术前2~4周开始系统性治疗,而EMERALD-1研究中,患者接受度伐利尤单抗或安慰剂治疗通常在首次TACE术后至少7天,在末次TACE术后至少14天开始使用贝伐珠单抗或安慰剂。
事实上,EMERALD-1研究的给药时间与此前2期试验安全性结局有关,不过本次EMERALD-1研究在TACE后延迟贝伐珠单抗给药的方式,似乎排除了安全性问题。因为研究显示,度伐利尤单抗+贝伐珠单抗+TACE组合的不良事件发生情况,与免疫治疗联合VEGF抑制剂(不含TACE)的不良事件类似。因此,关于TACE与基于免疫检查点抑制剂的联合用药的最佳用药时间,仍是临床需要持续探索的问题。
需要指出的是,尽管两项研究均证实TACE+免疫检查点抑制剂+VEGF抑制剂的方式,可改善肝癌患者PFS,但目前在总生存期方面的数据仍未成熟。LEAP-012研究的首次中期分析显示了TACE+仑伐替尼+帕博利珠单抗方案24个月总生存率更高的结果,但也还需更长时间的随访数据。EMERALD-1研究中总生存期也是关键次要终点,本次尚未报告相关数据。
《柳叶刀》发表的同期社论指出,基于这两项研究结果,临床可考虑在疾病早期阶段采用免疫检查点抑制剂联合用药的策略,因为相比于现在的疾病晚期用药策略,早期用药可能可以在患者身体和心理负担都较低时,更好地控制肿瘤。
参考资料
[1] Masatoshi Kudo, Zhenggang Ren, Yabing Guo, et al. Transarterial chemoembolisation combined with lenvatinib plus pembrolizumab versus dual placebo for unresectable, non-metastatic hepatocellular carcinoma (LEAP-012): a multicentre, randomised, double-blind, phase 3 study. The Lancet. Published January 8, 2025. DOI: 10.1016/S0140-6736(24)02575-3
[2] Bruno Sangro, Masatoshi Kudo, Joseph P Erinjeri, et al. Durvalumab with or without bevacizumab with transarterial chemoembolisation in hepatocellular carcinoma (EMERALD-1): a multiregional, randomised, double-blind, placebo-controlled, phase 3 study. The Lancet. Published January 8, 2025. DOI: 10.1016/S0140-6736(24)02551-0
[3] Florian P Reiter, Andreas Geier. TACE plus immune checkpoint inhibitor-based systemic therapies for hepatocellular carcinoma. The Lancet. Published January 8, 2025. DOI: 10.1016/S0140-6736(24)02680-1
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#肝癌# #免疫检查点抑制剂#
39 举报