STTT | RET融合阳性肺癌治疗新选择:HA121-28的I/II期临床试验结果
2025-03-05 daikun MedSci原创 发表于陕西省
HA121-28在RET融合阳性NSCLC患者中显示出令人鼓舞的抗肿瘤活性,尤其是在CCDC6-RET融合的患者中,客观缓解率和中位无进展生存期均优于KIF5B-RET融合的患者。
非小细胞肺癌(NSCLC)是全球癌症死亡的主要原因之一,占肺癌病例的 85% 左右。由于晚期诊断的普遍性,NSCLC 的 5 年生存率极低,仅为 7%。近年来,随着对 NSCLC 分子特征的深入了解,靶向治疗取得了突破性进展。酪氨酸激酶抑制剂(TKI)作为靶向治疗的基石,通过抑制异常受体酪氨酸激酶的活性,有效控制肿瘤生长和转移。RET 融合基因在多种实体瘤中表达,包括 1% 至 2% 的 NSCLC 患者。RET 融合导致 RET 酪氨酸激酶的组成性激活,从而促进肿瘤细胞增殖、存活、迁移和分化。既往研究表明,RET 融合 NSCLC 患者通常不吸烟,晚期诊断,PD-1 表达低,肿瘤突变负荷低。在一线化疗后进展时,二线和后续治疗的选择有限,存在未被满足的医疗需求。针对 RET 融合的靶向治疗是 NSCLC 治疗的重要进展。既往临床研究表明,多种多激酶抑制剂(如凡德他尼、卡博替尼和仑伐替尼)在 RET 融合 NSCLC 患者中展现出一定的抗肿瘤活性,但临床疗效相对有限,且治疗相关毒性较高。目前,普拉替尼和塞尔帕替尼两种新型选择性 RET 抑制剂已获批用于治疗 RET 融合阳性 NSCLC,并展现出优异的疗效。然而,所有患者最终都会对这些药物产生耐药性,耐药机制包括靶点内突变(如 KIF5B-RET G810C/S/R)和非靶点耐药(如 MET 扩增、PIK3CA 突变、PTEN 缺失等)。多靶点抑制剂 HA121-28 是一种具有潜力的多激酶抑制剂,主要针对 RET 融合基因,同时抑制血管内皮生长因子受体-2(VEGFR-2)、表皮生长因子受体(EGFR)和成纤维细胞生长因子受体 1-3(FGFR 1-3)。HA121-28 在临床前研究中展现出良好的抗肿瘤活性,并且在 1 期临床试验中展现出可耐受的安全性和初步的抗肿瘤活性。本研究旨在评估 HA121-28 在晚期实体瘤患者中的安全性、药代动力学特征,以及在 RET 融合阳性 NSCLC 患者中的初步疗效。

方法
这项研究是一项多中心、开放标签、单臂的I/II期临床试验。I期试验分为剂量递增和剂量扩展两部分,评估HA121-28的安全性、耐受性和药代动力学特性。II期试验则专注于评估HA121-28在RET融合阳性NSCLC患者中的疗效和安全性。纳入患者年龄 18-75 岁,患有不可切除的局部晚期或转移性 NSCLC,经二代测序证实存在 RET 融合基因,且既往至少接受过一种标准治疗的患者。在I期试验中,患者接受口服HA121-28,剂量范围为25至800 mg,采用21天用药/7天停药的方案,每28天为一个周期。在II期试验中,推荐剂量为450 mg,患者接受相同的治疗方案。主要终点包括I期的最大耐受剂量(MTD)和II期的客观缓解率(ORR)。次要终点包括无进展生存期(PFS)、总生存期(OS)和治疗相关不良事件(TRAEs)。
研究结果
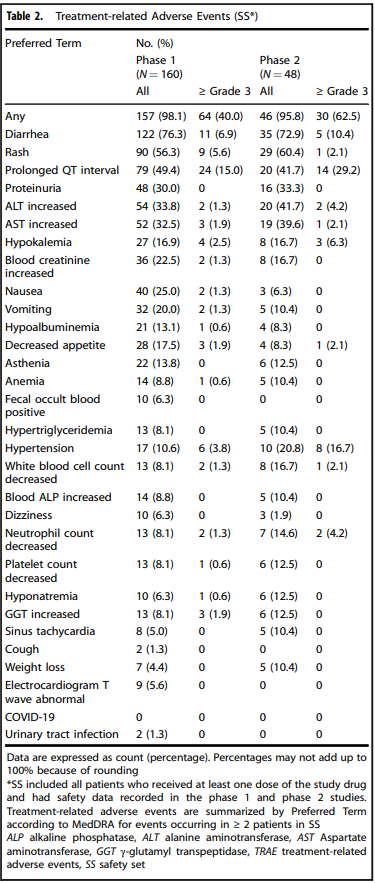
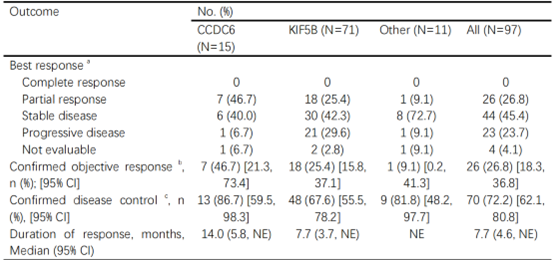
在I期试验中,共招募了162例晚期实体瘤患者,其中最常见的肿瘤类型为肺癌(67.5%),包括62例RET融合阳性的NSCLC患者。在II期试验中,共招募了48例RET融合阳性的NSCLC患者。总体而言,HA121-28在97例接受≥450 mg每日一次剂量的NSCLC患者中表现出令人鼓舞的疗效,客观缓解率为26.8%,中位无进展生存期为5.5个月。在携带 CCDC6-RET 融合的患者中,ORR 为 46.7%,中位缓解持续时间(DOR)为 14.0 个月。在携带 KIF5B-RET 融合的患者中,ORR 为 25.4%,中位 DOR 为 7.7 个月。在安全性方面,腹泻、皮疹和QT间期延长是最常见的治疗相关不良事件。在I期试验中,40.0%的患者经历了≥3级的治疗相关不良事件,而在II期试验中,这一比例为62.5%。值得注意的是,QT间期延长的发生率较高,需要在临床应用中密切监测。
结论
HA121-28在RET融合阳性NSCLC患者中显示出令人鼓舞的抗肿瘤活性,尤其是在CCDC6-RET融合的患者中,客观缓解率和中位无进展生存期均优于KIF5B-RET融合的患者。然而,QT间期延长的风险需要密切关注,并在临床应用中进行适当管理。未来的研究应进一步探索HA121-28在RET融合阳性NSCLC患者中的长期疗效和安全性,特别是在与其他药物的联合应用方面。
原始出处
Ruan, D.-Y., Huang, W.-W., Li, Y., Zhao, Y., Shi, Y., Jia, Y., ... & Zhao, H. (2025). Safety, pharmacokinetics and efficacy of HA121-28 in patients with advanced solid tumors and RET fusion-positive non-small-cell lung cancer: a multicenter, open-label, single-arm phase 1/2 trial. Signal Transduction and Targeted Therapy, 10(1), 62. https://doi.org/10.1038/s41392-025-02155-5.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#Ⅰ/Ⅱ期研究# #HA121-28# #RET融合阳性NSCLC#
24 举报