青海大学STTT:探索三阴性乳腺癌的临床用药方案
2025-02-09 BioMed科技 BioMed科技 发表于陕西省
三阴性乳腺癌异质性高、侵袭性强。NeoSAC二期试验探索阿帕替尼联合信迪利单抗和化疗用于早期TNBC新辅助治疗的效果。
三阴性乳腺癌(TNBC)是一种高度异质性和侵袭性强的乳腺癌亚型,与较高的复发风险、远处转移以及较差的预后相关。在新辅助治疗领域,早期TNBC通常对化疗有较高的响应率,从而显著提高了病理完全缓解(pCR)率和长期生存结果。因此,新辅助治疗在早期TNBC中扮演着越来越重要的角色,用于降低肿瘤分期并改善生存。
传统上,蒽环类药物和紫杉类药物是TNBC的新辅助治疗首选。然而,近年来的研究引入了多种有前景的替代方案,包括铂类药物为基础的化疗、免疫检查点抑制剂(ICIs)、聚腺苷二磷酸核糖聚合酶(PARP)抑制剂、抗血管生成疗法和抗体药物偶联物等,这些新疗法拓宽了TNBC的治疗选择范围。其中,铂类药物显著提高了pCR率,并在国际指南中被不同程度地推荐。ICIs,尤其是帕博利珠单抗,显示出卓越的疗效,显著提高了pCR率和长期生存率,也被纳入了最近的指南。
然而,尽管ICIs联合化疗显著提高了TNBC的pCR率,但仍有大部分患者无法达到pCR,这表明需要进一步优化治疗策略以提高病理反应和生存率。此外,肿瘤血管生成和免疫调节之间存在密切的相互作用。异常的肿瘤血管通过缺氧和酸中毒的肿瘤微环境以及促血管生成的细胞因子,将炎症细胞极化为免疫抑制状态,而免疫抑制细胞也可以诱导血管生成。这种肿瘤血管生成和免疫抑制之间的交叉作用导致了一个恶性循环,干扰了抗肿瘤免疫治疗的效果。因此,通过抗血管生成药物来改善肿瘤血管,从而增强抗肿瘤免疫治疗的疗效,具有重要的临床意义。
青海大学附属医院赵久达、刘震和中国医学科学院北京协和医学院马飞等人开展了NeoSAC二期临床试验,旨在探索在早期TNBC的新辅助治疗中,将阿帕替尼(一种血管内皮生长因子受体2(VEGFR2)酪氨酸激酶抑制剂)加入到信迪利单抗(一种抗程序性死亡1抗体)以及基于卡铂和紫杉醇的化疗方案中的疗效、安全性和生物标志物。相关内容以“Neoadjuvant apatinib addition to sintilimab and carboplatin-taxane based chemotherapy in patients with early triple-negative breast cancer: the phase 2 NeoSAC trial”为题发表在《Signal Transduction and Targeted Therapy》上。

【主要内容】
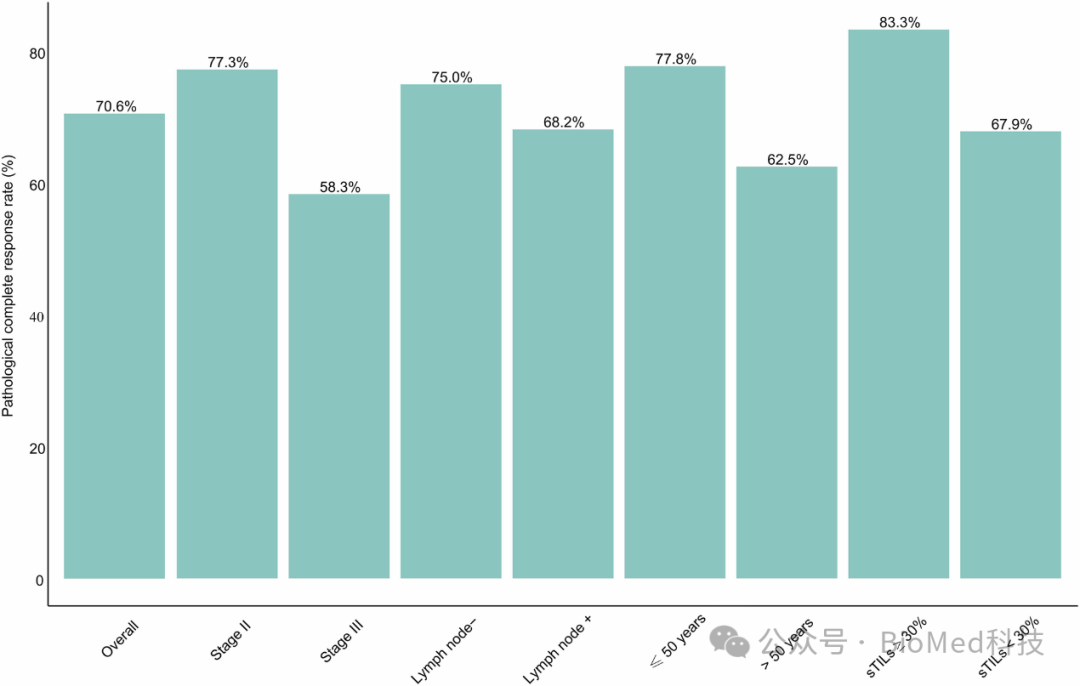
图1:pCR率及亚组分析
上图展示了在34例接受治疗的患者中,24例(70.6%)达到了pCR,即在乳腺和腋窝淋巴结中均未发现侵袭性癌细胞残留。亚组分析表明,早期疾病阶段(II期)、年轻(≤50岁)、无淋巴结转移以及肿瘤浸润性淋巴细胞(sTILs)≥30%的患者具有更高的pCR率。
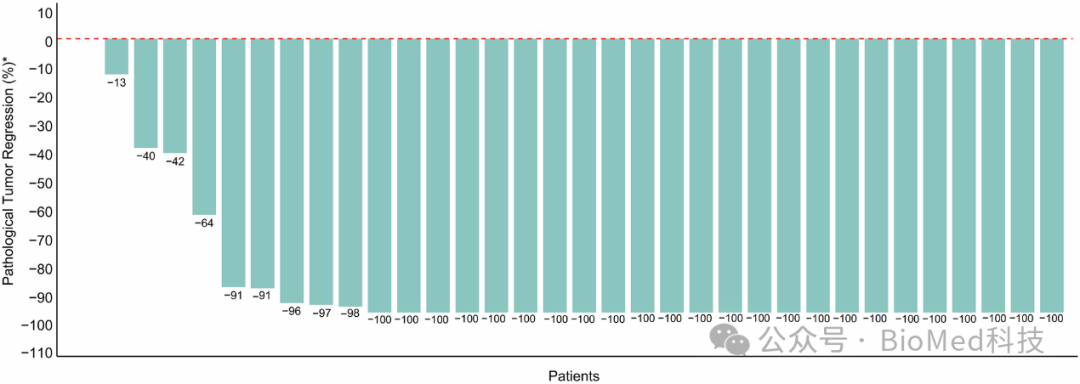
图2:手术切除后的病理肿瘤缓解情况
在33例可评估的患者中,根据Miller-Payne评分系统评估了病理肿瘤缓解情况。结果显示,72.7%的患者达到了pCR,表明在手术切除后的病理评估中,大部分患者对新辅助治疗有良好的反应。
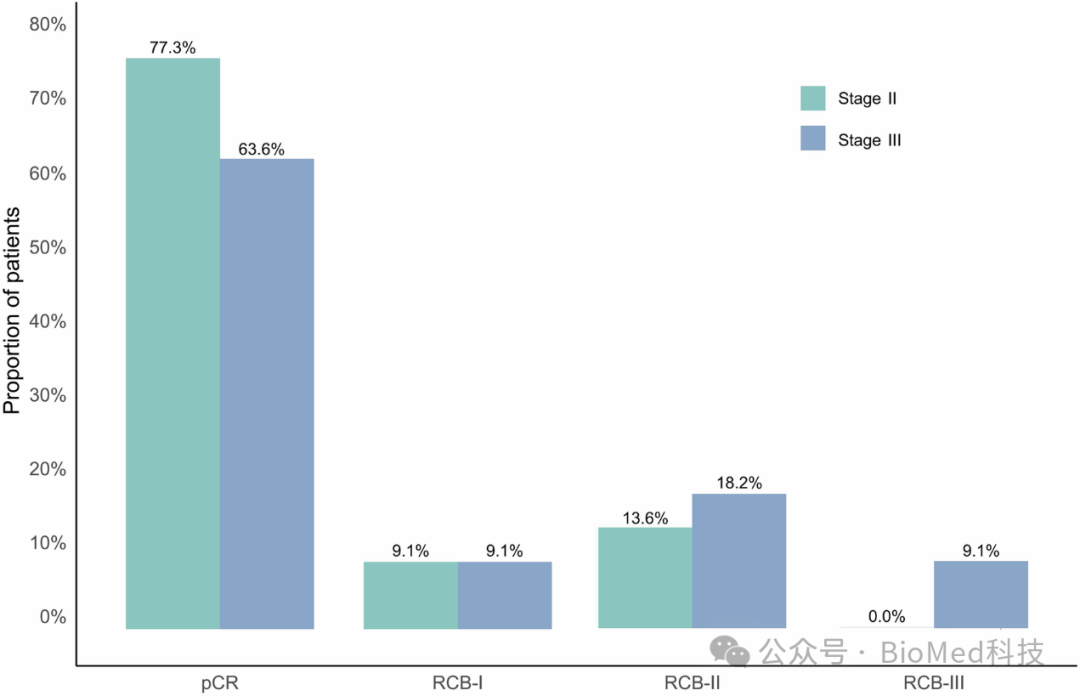
图3:不同临床分期的残余癌症负担(RCB)分析
根据临床分期(II期和III期)分析了RCB情况。结果显示,II期患者的pCR率高于III期患者,且II期患者在RCB-I(无或轻微残余疾病)的比例也更高。这表明早期疾病阶段的患者对新辅助治疗的反应更好,可能与肿瘤的生物学特性和治疗敏感性有关。
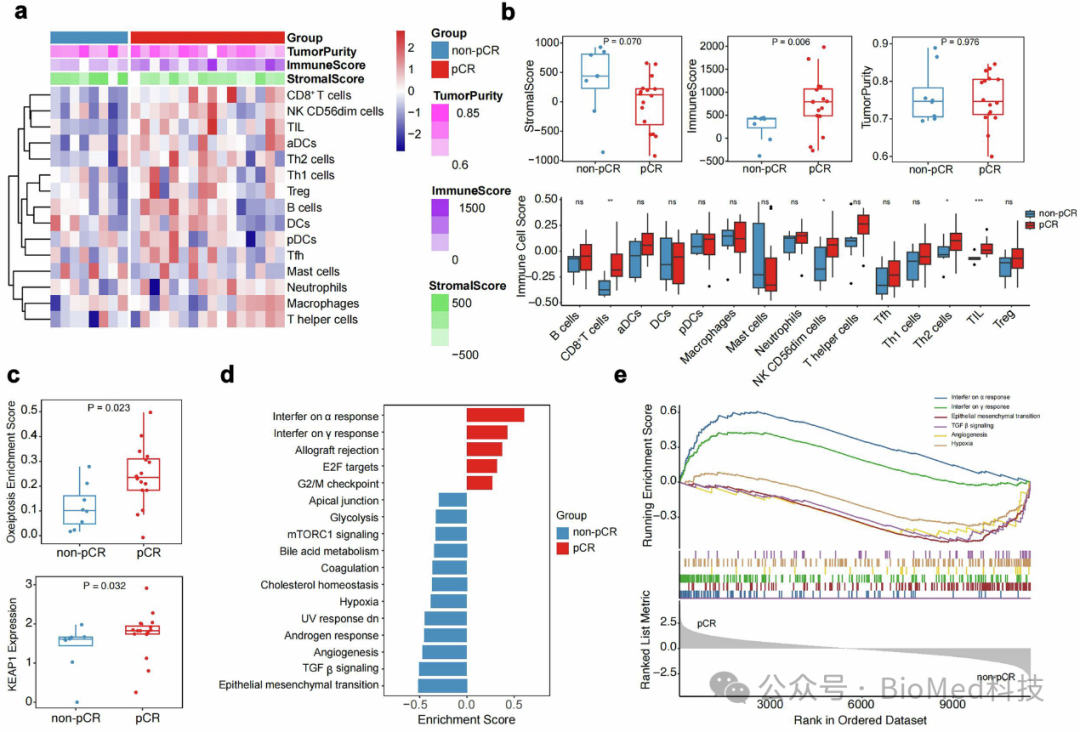
图4:治疗前基线免疫微环境的比较分析
作者比较了达到pCR和未达到pCR的患者在治疗前的基线免疫微环境特征。结果显示,高ImmuneScore、免疫细胞浸润以及干扰素相关通路的富集与pCR相关。
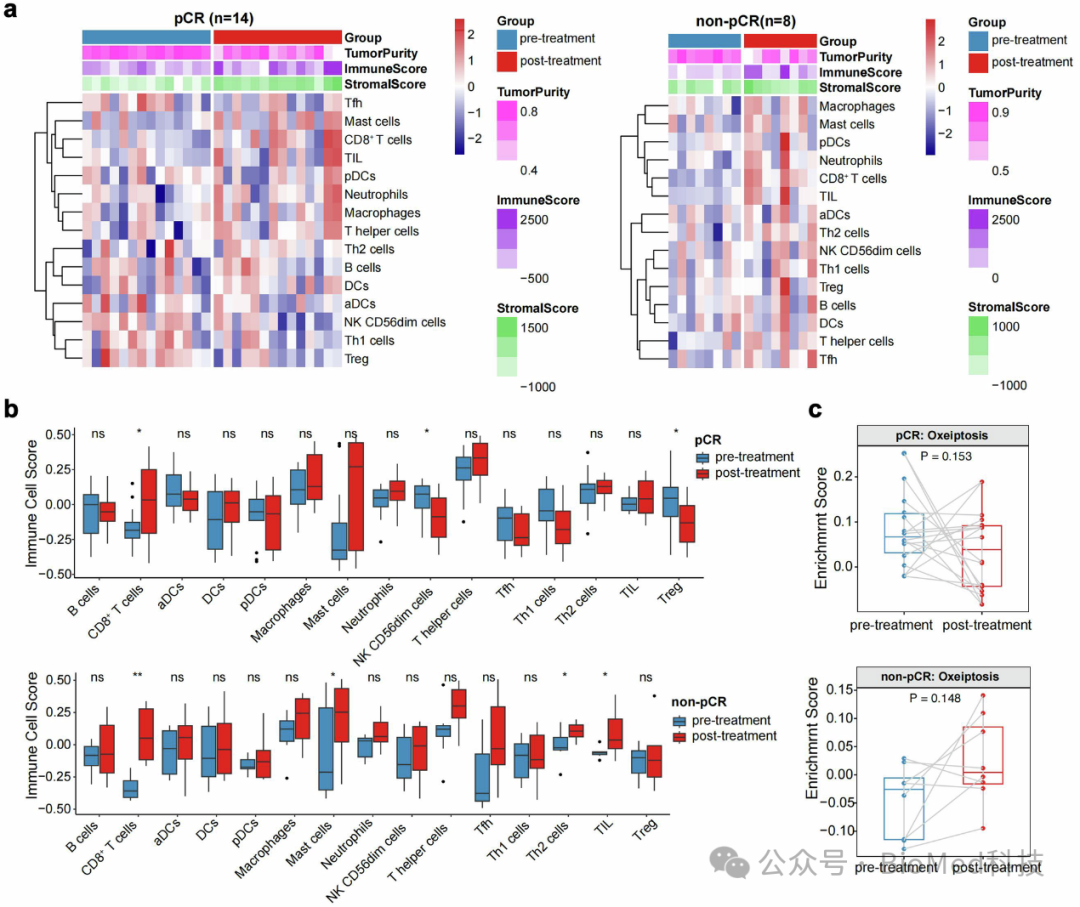
图5:治疗前后免疫微环境的动态变化比较
pCR组在治疗后表现出特定免疫细胞亚群的上调,激活了肿瘤微环境,而非pCR组则表现出相反的变化趋势。此外,氧化应激诱导的细胞死亡(oxeiptosis)评分在pCR组治疗后降低,而在非pCR组中增加,提示oxeiptosis可能与治疗反应相关,为未来的研究提供了新的方向。
【全文总结】
本文报告了NeoSAC二期临床试验的结果,旨在评估阿帕替尼联合信迪利单抗及基于卡铂和紫杉醇的化疗方案在早期三阴性乳腺癌(TNBC)新辅助治疗中的疗效和安全性。研究共纳入34例患者,结果显示病理完全缓解(pCR)率为70.6%,残余癌症负担(RCB)0-I率为79.4%,客观缓解率(ORR)为100%。治疗相关不良事件主要为血液学毒性,但未出现治疗相关死亡。中位随访39.1个月后,36个月无病生存(DFS)率为94.1%。生物标志物分析表明,高ImmuneScore、免疫细胞浸润和干扰素相关通路的富集与pCR相关,而氧化应激诱导的细胞死亡(oxeiptosis)评分与pCR的可能性相关。研究结果表明,阿帕替尼联合信迪利单抗及化疗方案在早期TNBC中显示出良好的临床活性和可管理的安全性,值得进一步研究。
原文链接:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#三阴性乳腺癌# #新辅助治疗#
28 举报