全球首个实体瘤 CAR-T 疗法登顶 Lancet!中国团队证实CLDN18.2 靶向疗法显著延长胃癌或胃食管结合部癌患者无进展生存期
2025-06-04 MedSci原创 MedSci原创 发表于上海
这是全球首个针对实体瘤的CAR T细胞疗法随机对照试验。satri-cel治疗显著延长了既往接受过治疗的CLDN18.2阳性晚期G/GEJC患者的无进展生存期和总生存期。
胃癌或胃食管结合部癌(G/GEJC)位列全球癌症发病率与死亡率第五位。这类癌症在晚期时治疗难度大,特别是对二线乃至后续治疗反应不佳的患者而言,其生存期往往极为有限。
近日,由北京大学肿瘤医院的沈琳教授团队设计主导的全球首个CLDN18.2 CAR-T胃癌随机对照研究的阳性结果正式发布于国际权威学术期刊Lancet。结果显示,以靶向 CLDN18.2 的自体 CAR-T 细胞疗法Satricabtagene autoleucel(Satri-cel;亦称为CT041)显著延长了既往接受过治疗的CLDN18.2阳性晚期G/GEJC患者的无进展生存期,且总生存期也有临床意义上的延长。令人激动的是,该研究结果也荣登 Nature 顶刊官网头条。

CAR-T 疗法,自问世以来,在血液肿瘤治疗领域可谓成绩斐然。通过对患者自身 T 细胞进行基因改造,使其能够精准识别并攻击肿瘤细胞,CAR-T 疗法已成功获批用于白血病、淋巴瘤等多种血液类恶性肿瘤的治疗。然而,当将这一疗法应用于实体瘤时,却遭遇了重重阻碍。实体瘤复杂的微环境、缺乏特异性且安全有效的靶点等问题,使得 CAR-T 疗法难以发挥其应有的作用,众多临床试验结果均不尽人意。
Claudin-18 isoform 2(CLDN18.2)的出现,为实体瘤治疗带来了新的契机。CLDN18.2是正常组织紧密连接中重要的一种蛋白质,在多种消化道肿瘤中存在高表达,尤其在G/GEJC,约40%的患者呈中度至高度表达。目前,针对CLDN18.2的单克隆抗体佐妥昔单抗在我国获批,联合含氟尿嘧啶类和铂类药物化疗用于CLDN18.2阳性、人表皮生长因子受体2(HER2)阴性的局部晚期不可切除或转移性胃或胃食管交界处(GEJ)腺癌患者的一线治疗。
本研究是一项在中国 24 个研究中心开展的开放标签、多中心、随机对照的2期临床试验(CT041-ST-01)。患者纳入标准包括:年龄18至75岁、病理确诊的晚期G/GEJC、CLDN18.2阳性(免疫组化表达强度≥2+且阳性肿瘤细胞≥40%)、HER2阴性、至少接受过二线治疗且失败、至少有一个可测量病灶等。
共纳入156名患者,并以2:1比例被随机分配至satri-cel组(n=104)或医生选择治疗组(TPC)(n=52)。Satri-cel组患者接受最多三次satri-cel输注,剂量为250×10⁶细胞;TPC组患者接受医生选择的标准治疗药物(包括纳武单抗、紫杉醇、多西他赛、伊立替康或阿帕替尼),若病情进展或药物不耐受可接受后续satri-cel治疗。研究时间为2022年3月22日至2024年7月29日,主要终点是由独立评审委员会评估的无进展生存期(PFS)。
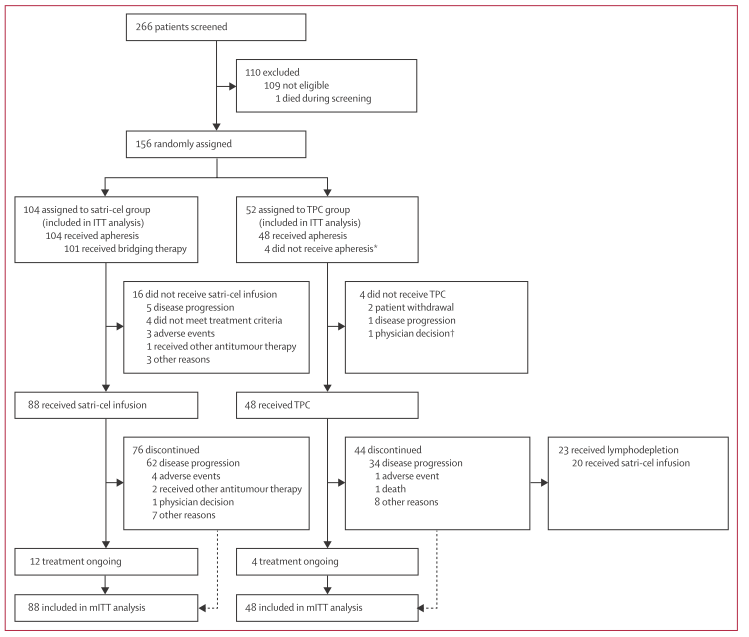
结果显示,在基线特征方面,两组患者基本平衡,中位年龄均为52岁,男性占比约56%,大多数患者为胃腺癌,约70%的患者既往接受过二线治疗,约27%的患者既往接受过三线或更多治疗。
在意向治疗(ITT)人群中,satri-cel组中位PFS为3.25个月,TPC组为1.77个月,表明satri-cel显著延长了PFS。在总生存期(OS)方面,satri-cel组中位OS为7.92个月,TPC组为5.49个月。相比标准疗法,satri-cel 将患者的中位总生存期延长了 44%。此外,satri-cel组客观缓解率(ORR)显著提高为 22%,TPC组ORR仅为4%。
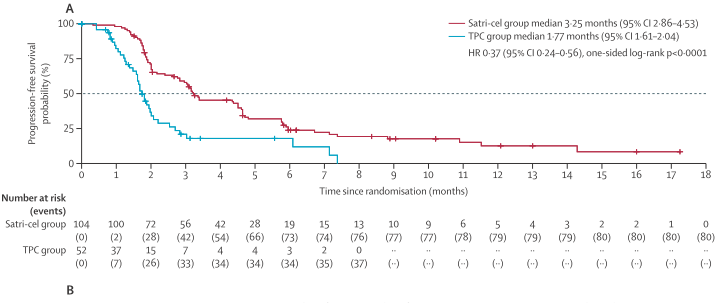
无进展生存期的比较
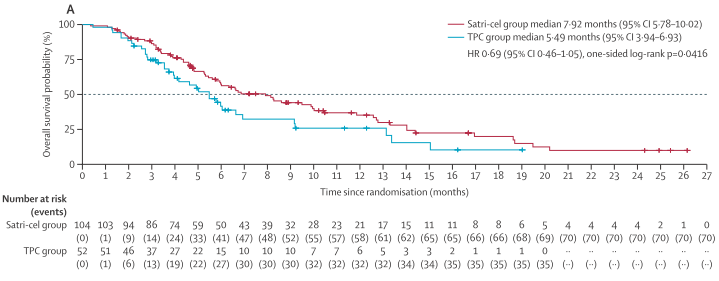
总生存期的比较
在安全性方面,satri-cel组所有患者均发生治疗相关不良事件,其中99%的患者发生3级或更高级别的不良事件,最常见的是淋巴细胞计数减少、白细胞计数减少和中性粒细胞计数减少,95%的患者出现细胞因子释放综合征,但大多数为1级或2级;TPC组92%的患者发生治疗相关不良事件,63%的患者发生3级或更高级别的不良事件。
综上所述,这是全球首个针对实体瘤的CAR T细胞疗法随机对照试验。satri-cel治疗显著延长了既往接受过治疗的CLDN18.2阳性晚期G/GEJC患者的无进展生存期和总生存期。尽管satri-cel不良事件发生率较高,但大多数不良事件是可控的,且未观察到长期严重不良事件。这些结果表明satri-cel有望成为这类患者的新三线治疗选择。
参考资料
Claudin-18 isoform 2-specific CAR T-cell therapy (satri-cel) versus treatment of physician's choice for previously treated advanced gastric or gastro-oesophageal junction cancer (CT041-ST-01): a randomised, open-label, phase 2 trial.Qi, Changsong et al.The Lancet, Volume 0, Issue 0
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#胃癌# #胃食管结合部癌# #CLDN18.2 靶向疗法# # CAR-T 疗法#
27 举报