新路径!皮下注射Blinatumomab治疗复发难治性B-ALL获益显著,疗效安全俱佳
2025-06-26 MedSci原创 MedSci原创 发表于上海
此次研究首度系统展示了Blinatumomab皮下注射的疗效、安全性及药代动力学数据,表明其在复发难治性B-ALL患者中展现出较传统静脉给药更为优异的缓解率以及深度分子缓解。
B细胞急性淋巴细胞白血病(B-ALL)过去因高复发率和治疗失败率导致患者预后不佳。近年来,靶向治疗如双特异性抗体(bispecific antibodies)、嵌合抗原受体T细胞疗法(CAR T)及抗体偶联药物显著改善了部分患者的生存预后。然而,仍有大量患者因年龄、合并症或既往治疗耐药而无法从现有疗法中获益。
Blinatumomab是一种CD19/CD3双特异性T细胞接合器(BiTE),能够同时连接CD3阳性细胞毒性T细胞与CD19阳性B细胞,诱导T细胞清除白血病细胞。目前连续静脉输注(cIV)给药模式虽有效,但给药延续时间长,且伴随较多血管相关不良反应。为简化给药流程及提升患者便捷性,皮下注射(SC)方式被开发用于评估更高暴露量和潜在的疗效优势。
近日,发表在Lancet Haematology上的一项多中心单臂1/2期临床研究,系统评估了两种皮下注射Blinatumomab剂量方案在成年复发或难治性B细胞急性淋巴细胞白血病患者中的安全性及疗效,筛选出推荐用于后续Ⅱ期试验的最佳剂量。本文将围绕该研究的设计、结果及临床意义进行详细解读。
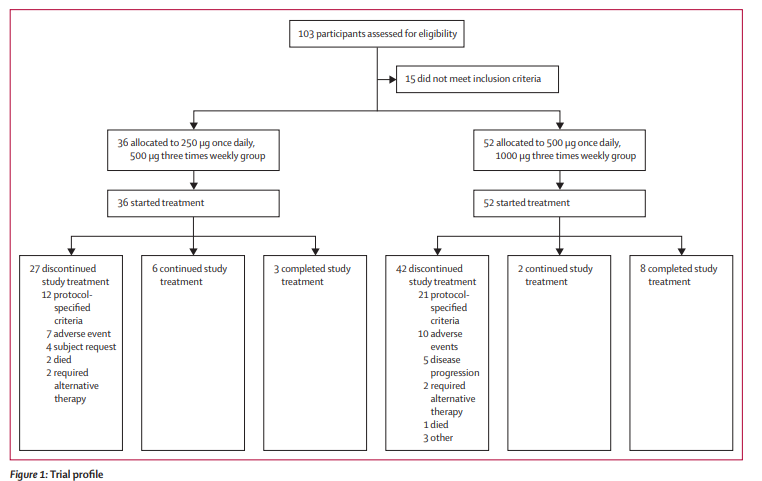
本研究为一项多中心、单臂、开放标签1/2期临床试验,在11个国家44家医院招募了88名年龄≥18岁、骨髓幼稚细胞≥5%、并经确诊的复发或难治性B-ALL患者。试验评估两种皮下注射剂量候选方案:
- 250μg每日1次(第1周),随后500μg每周3次(第1/2方案)
- 500μg每日1次(第1周),随后1000μg每周3次(第2/2方案)
每个治疗周期含4周用药加1周间歇,患者最多接受5个周期。中期主要终点为前两周期内完全缓解(CR)或部分血液学恢复的完全缓解(CRh)率。药代动力学及安全性也被系统评估。所有患者均记录不良事件,特别关注细胞因子释放综合征(CRS)及免疫效应细胞相关神经毒性综合征(ICANS)。
主要结果详解
基线特征与治疗依从性
两组患者基线特征均衡,均为重度复发和多线治疗失败患者,体现出真实世界高风险群体的代表性。
疗效评价
- CR或CRh率分别为250μg/500μg组75%(27/36)和500μg/1000μg组79%(41/52)。
- 获得CR/CRh的患者中,91%达成分子学(MRD)阴性,显示深度缓解。
- 癌症复发率低,治疗后≥3个月随访期内,75-72%的患者无复发。
- RA及更晚期治疗背景患者同样受益,包括既往接受过cIV Blinatumomab、CAR-T或其他靶向治疗。

安全性分析
- 所有患者均出现至少一种治疗相关不良事件,常见3-4级不良事件包括:中性粒细胞减少(22%)、CRS(20%)、ICANS(17%)和贫血(14%)。
- CRS多为1-2级,发生于治疗首日,平均持续时间5天,多数接受激素、支持治疗缓解,无需停药。
- ICANS在两组均有发生(7%患者3-4级),但均有效控制,仅7%因神经毒性停药,无死亡病例与治疗直接相关。
- 药代动力学显示两剂量暴露呈剂量比例性增加,皮下注射浓度峰值出现较晚(6-12h),且血药浓度高于传统静脉滴注方案,半衰期约8-12h,利于更灵活给药安排。
总生存
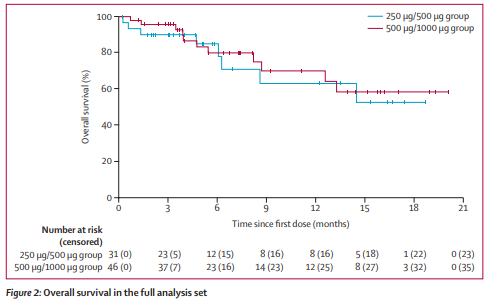
- 截止数据切点,中位随访5个月,尚未达到中位生存期。
- 12个月总生存率68%,缓解患者生存率高达82%。
- 约1/3缓解患者继发行造血干细胞移植,其他患者仅靠Blinatumomab单药维持较好疗效。
研究讨论及价值评析
此次研究首度系统展示了Blinatumomab皮下注射的疗效、安全性及药代动力学数据,表明其在复发难治性B-ALL患者中展现出较传统静脉给药更为优异的缓解率以及深度分子缓解。
皮下注射方式不仅显著提高了患者的给药便捷度,减少了对中心静脉留置管及输注泵的依赖,降低了相关感染风险,也缩短了给药时间和患者留院负担,未来具备推广至门诊甚至居家医疗的潜力。高药物暴露和更合理的药代动力学特征可能是促进疗效提升的关键。
安全事件与既知的Blinatumomab静脉给药相似,无新增严重安全信号。尽管CRS及ICANS仍需重视,绝大多数可通过早期识别和支持治疗有效管理,且无治疗相关死亡,显示较好的耐受性。对于已接受CAR-T及多线靶向治疗失败的患者,皮下注射Blinatumomab仍表现出强有力的挽救效果,拓展了该药物的临床适用范围。
Blinatumomab的这一给药创新也为未来B-ALL及其他B细胞相关血液恶性肿瘤的治疗模式改革提供了选择,助力临床医生在个体化治疗策略中增加有力工具。
下一阶段Ⅱ期试验将继续探索推荐剂量(250μg/500μg方案),验证更长远疗效及安全数据,优化不良事件管理策略,为临床应用铺路。
梅斯点评
梅斯张博士:这项研究为复发难治性B-ALL患者引入了一个极具临床实用价值的治疗选择。传统Blinatumomab的连续静脉点滴给药制约着患者的生活质量与治疗依从性,而皮下注射方案的成功,不仅为患者带来了更大便利,也可能提升治疗依从度和疗效深度。这代表了免疫治疗药物给药方式创新的一个极佳范例,未来还可探讨其与其他靶向疗法及免疫细胞疗法的联合应用。
梅斯小编补充:虽然此研究为非随机设计,随访时间尚短,但其高响应率和安全可控的特性足以引起关注。未来应加强对长期生存结果、免疫记忆效应及MRD监测的深入解析,同时研究各类患者亚群,尤其先前接受CAR-T治疗的患者,用以指导临床精准治疗策略。
原始出处
Elias Jabbour et al. Subcutaneous blinatumomab in adults with relapsed or refractory B-cell acute lymphoblastic leukaemia: post-hoc safety and activity analysis from a multicentre, single-arm, phase 1/2 trial. Lancet Haematol. Published online June 15, 2025. https://doi.org/10.1016/S2352-3026(25)00144-9
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#Blinatumomab# #B细胞急性淋巴细胞白血病#
23 举报