J Hepatol :上海营养与健康研究所李于团队首次揭示了肝细胞中通过蛋白磷酸酶PPP6C调节MASH发育的新信号轴!
2025-02-18 iNature iNature 发表于陕西省
该研究表明蛋白磷酸酶6通过mTORC1通路调节代谢功能障碍相关的脂肪性肝炎。
代谢功能障碍相关脂肪性肝炎(MASH)是一种严重的慢性肝病,治疗方法有限。尽管成纤维细胞生长因子21 (FGF21)类似物在多项临床前和临床研究中显示出对MASH有希望的治疗益处,但其潜在机制仍不清楚。
2025年2月10日,中国科学院上海营养与健康研究所李于团队在Journal of Hepatology在线发表题为“Protein phosphatase 6 regulates metabolic dysfunction-associated steatohepatitis via the mTORC1 pathway”的研究论文,该研究表明蛋白磷酸酶6通过mTORC1通路调节代谢功能障碍相关的脂肪性肝炎。
研究确定丝氨酸和苏氨酸磷酸酶PPP6C是FGF21的直接靶点。肝脏PPP6C缺陷加速喂食AMLN饮食或CDA-HFD的小鼠的MASH进展,这阻断了FGF21对MASH的作用。从机理上讲,PPP6C足以在FGF21处理后与辅助受体βKlotho相互作用,直接去磷酸化Ser939和Thr1462处的结节性硬化症2 (TSC2 ),从而抑制mTORC1并促进TFE3和Lipin1的核进入。在MASH受试者的肝脏中,PPP6C的表达水平降低,而TSC2磷酸化水平升高。这些结果定义了肝细胞中FGF21信号的基本机制,并证明靶向PPP6C可能具有治疗MASH的治疗潜力。

代谢功能障碍相关的脂肪性肝病(MASLD),以前称为非酒精性脂肪性肝病(NAFLD),正在成为最常见的慢性肝病,影响全球约24%的成年人。代谢功能障碍相关脂肪性肝炎(MASH),以前称为非酒精性脂肪性肝炎(NASH),是一种更严重的阶段,以肝损伤、炎症和纤维化为特征,增加了更严重的肝硬化和肝细胞癌(HCC)的风险,是肝移植的主要原因。肝细胞中过量脂滴的积聚是肝脂肪变性的标志,而应激诱导的脂肪肝细胞损伤和死亡是MASH发病机制的核心。受损或死亡的肝细胞进一步引发介质,放大炎症细胞或肝星状细胞中的炎症和纤维化信号,并促进MASH进展。尽管对肝细胞中控制代谢和细胞死亡的调节网络进行了广泛的探索,但MASH的临床治疗策略仍然有限。
成纤维细胞生长因子21 (FGF21)及其类似物对MASH的保护作用已经在临床前和临床研究中得到证实。在MASH小鼠模型中,重组FGF21蛋白或类似物改善了脂肪变性、炎症和纤维化。在临床试验中,FGF21类似物pegbelfermin、efruxifermin或pegozafermin治疗显著改善了MASH患者的肝脂肪含量和肝硬度,降低了肝损伤和纤维化标志物的血浆水平。此外,NGM313,FGF21受体复合物FGF受体1 (FGFR1)/βKlotho的激活剂,显著降低了肥胖非糖尿病受试者的肝脏脂肪含量。然而,FGF21信号是如何传导和调节MASH的,以及肝细胞是否是FGF21的主要药理学靶点仍然是未知的。
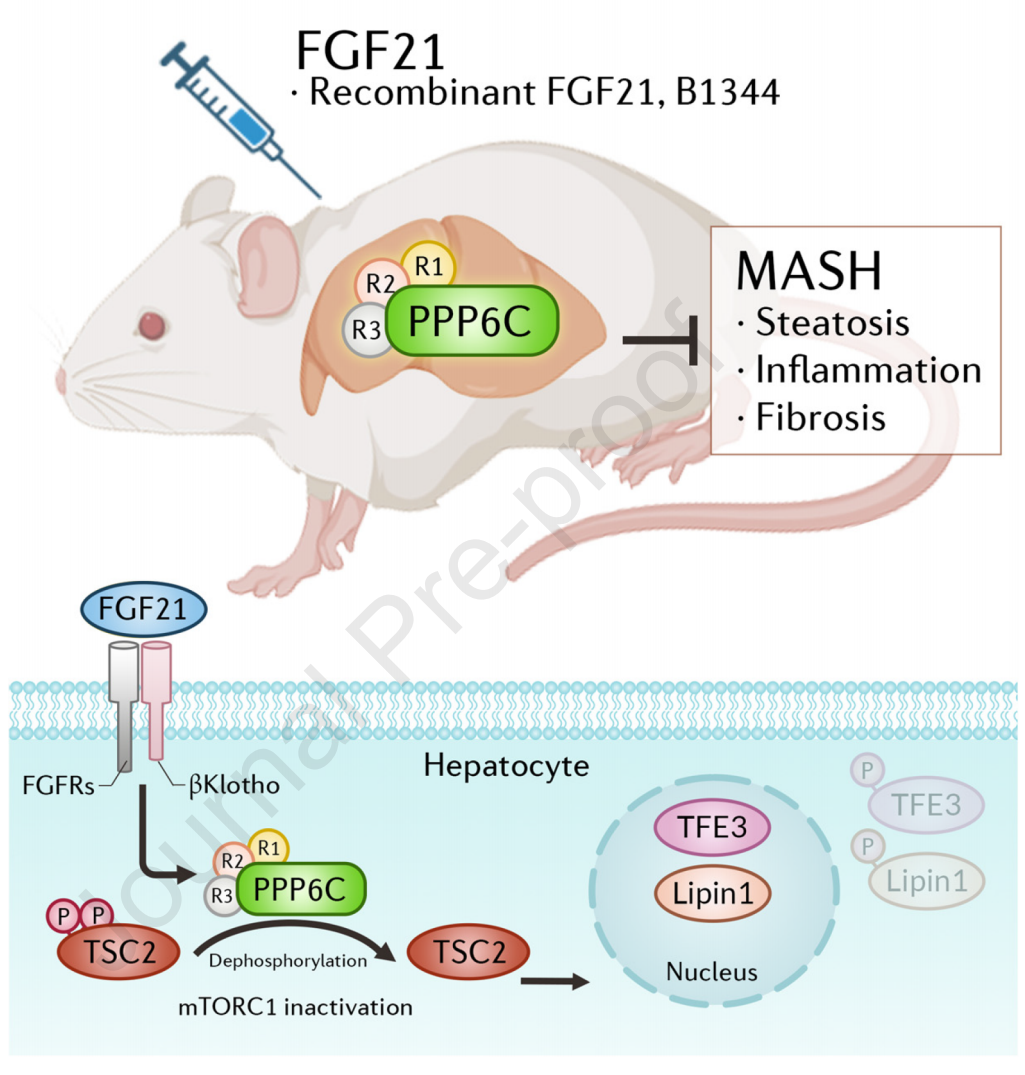
机理模式图(图源自Journal of Hepatology )
这项研究首次揭示了肝细胞中通过蛋白磷酸酶PPP6C调节MASH发育的新信号轴。具体来说,肝脏FGFRs/βKlotho受体感知细胞外FGF21刺激,并随后激活PPP6C复合物。PPP6C直接使TSC2在Ser939和Thr1462去磷酸化,从而抑制mTORC1。TFE3和Lipin1从细胞质转运到细胞核,在细胞核中它们抑制脂质合成基因的转录,但促进脂肪酸氧化基因的转录,有助于MASH的改善。这项研究表明,针对PPP6C活性的药理学方法、遗传或代谢因素可能为治疗肝纤维化和MASH提供有吸引力的前景。
参考消息:
https://www.journal-of-hepatology.eu/article/S0168-8278(25)00079-0/fulltext#au18
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#脂肪性肝炎# #蛋白磷酸酶6#
30 举报