JAMA Neurology:更汀芦单抗治疗早期阿尔茨海默病患者淀粉样相关影像异常风险全景解析
2025-06-24 吾乃喵大人 MedSci原创 发表于上海
本研究系统揭示了更汀芦单抗治疗早期AD患者ARIA尤其是ARIA-E的风险因子及病程特征,丰富了对抗Aβ单抗治疗安全性的认知。
研究亮点
- APOE ε4等遗传因素、阿尔茨海默病相关β淀粉样蛋白(Aβ)病理严重度及脑血管共病是更汀芦单抗治疗中ARIA-脑水肿(ARIA-E)的重要风险因素。
- 更汀芦单抗治疗中约25%的患者发生ARIA-E,但大多数ARIA-E对长期认知和功能无负面影响。
- ARIA的临床监测和个体化风险评估将在抗Aβ单抗的安全管理中发挥关键作用。
研究核心简介
本文报道了来自两项全球多中心、随机、双盲、安慰剂对照的III期GRADUATE I/II临床试验及其公开标签延伸研究PostGraduate中,对更汀芦单抗治疗早期阿尔茨海默病患者中淀粉样相关影像异常(ARIA)的系统分析。研究涵盖了近2000名患者,平均治疗时间超过两年,首次详尽刻画了ARIA的临床和影像学特征、发生时间、复发率、风险因素及其对认知和功能结局的影响。相关研究成果发表于JAMA Neurology。

背景介绍
阿尔茨海默病(AD)的主要病理过程之一是脑内Aβ蛋白的累积沉积。近年来,针对Aβ的单克隆抗体药物(如lecanemab、donanemab)展示出显著的清除Aβ斑块能力,并获得FDA批准,用于早期症状性AD的治疗。然而,这类药物的主要副作用为淀粉样相关影像异常(Aura-Related Imaging Abnormalities,ARIA),具体分为血管性脑水肿/脑实质液位(ARIA-E)及微出血/表层铁质沉积(ARIA-H)。ARIA的发生既可能源自疾病自身脑血管病变,也与抗Aβ抗体介导的免疫反应密切相关,并可能引起神经系统症状甚至严重事件。为优化临床应用,亟需明晰ARIA的相关风险因素、病程及长期结局,为安全用药提供指导。
方法学简述
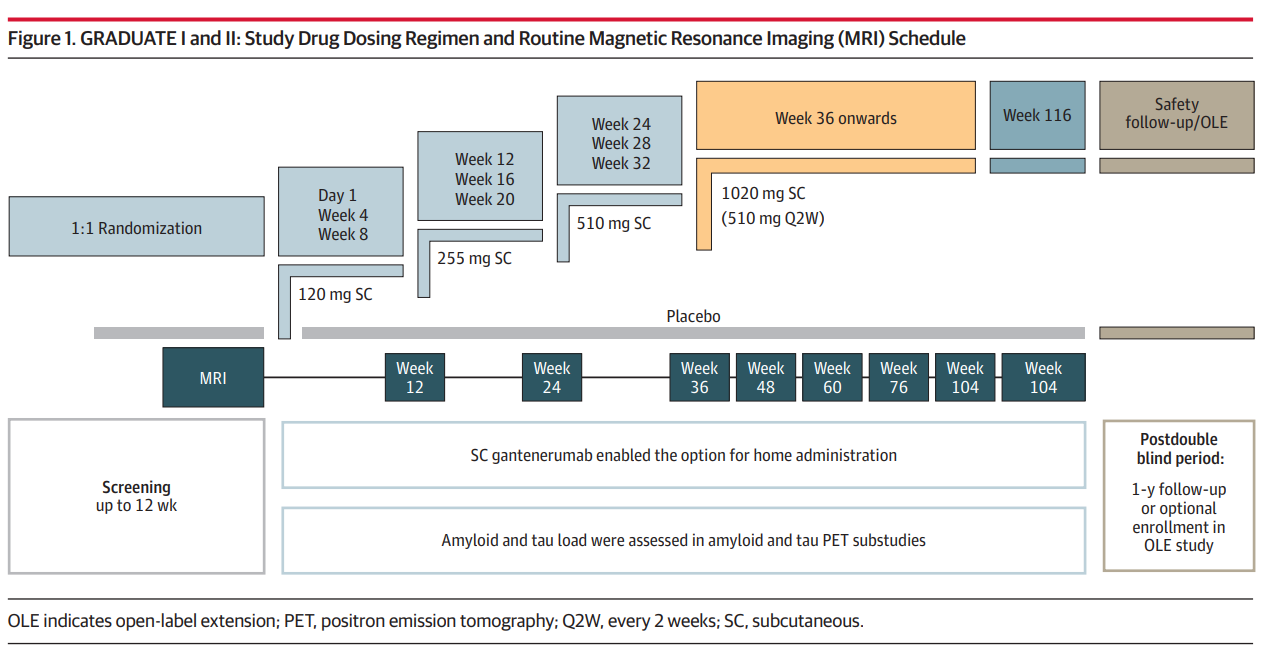
GRADUATE I/II两项Ⅲ期临床试验共招募1965名年龄50-90岁、具CTF (cerebrospinal fluid) Aβ42阳性及早期认知障碍或轻度AD诊断的患者,随机分配接受更汀芦单抗或安慰剂治疗,疗程116周,设有9个月的剂量渐进增量方案以降低ARIA风险。研究中,定期采用MRI监测ARIA表现,包括流体衰减反转恢复序列(FLAIR)用于ARIA-E检测,铁敏感序列(GRE/T2或SWI)用于检测ARIA-H,并结合临床症状评估定义“症状性ARIA-E”。
研究结果详解
-
患者基线特征
共1939名患者构成MRI安全评估人群,均衡性良好,平均年龄71.7岁,女性占57%。APOE ε4等位基因携带者约66%,其中异合子占约50%,纯合子17%。基线时约10%的更汀芦单抗患者存在微出血或表层铁沉积。 -
ARIA发生率及时间特征
更汀芦单抗组ARIA-E发生率为24.9%,ARIA-H为22.9%。绝大部分首次ARIA-E事件(约86%)发生于治疗开始后的64周内,但最长可延迟至168周。纯合子APOE ε4携带者ARIA-E发生比例最高(47.8%),明显高于异合子(24.5%)及非携带者(13.1%)。 -
ARIA-E症状及严重程度
约20%的ARIA-E患者出现神经系统相关症状,最常见为头痛、眩晕及认知混乱。严重症状(例如癫痫发作)占1%左右。症状出现率与APOE ε4等位基因数量呈正相关,但在发生ARIA-E的患者中,症状比例与APOE ε4拷贝数无显著关联。严重症状的ARIA-E普遍表现出更高BGTS影像评分,显示病灶范围大、程度重;同时症状性ARIA-E更常伴发ARIA-H。 -
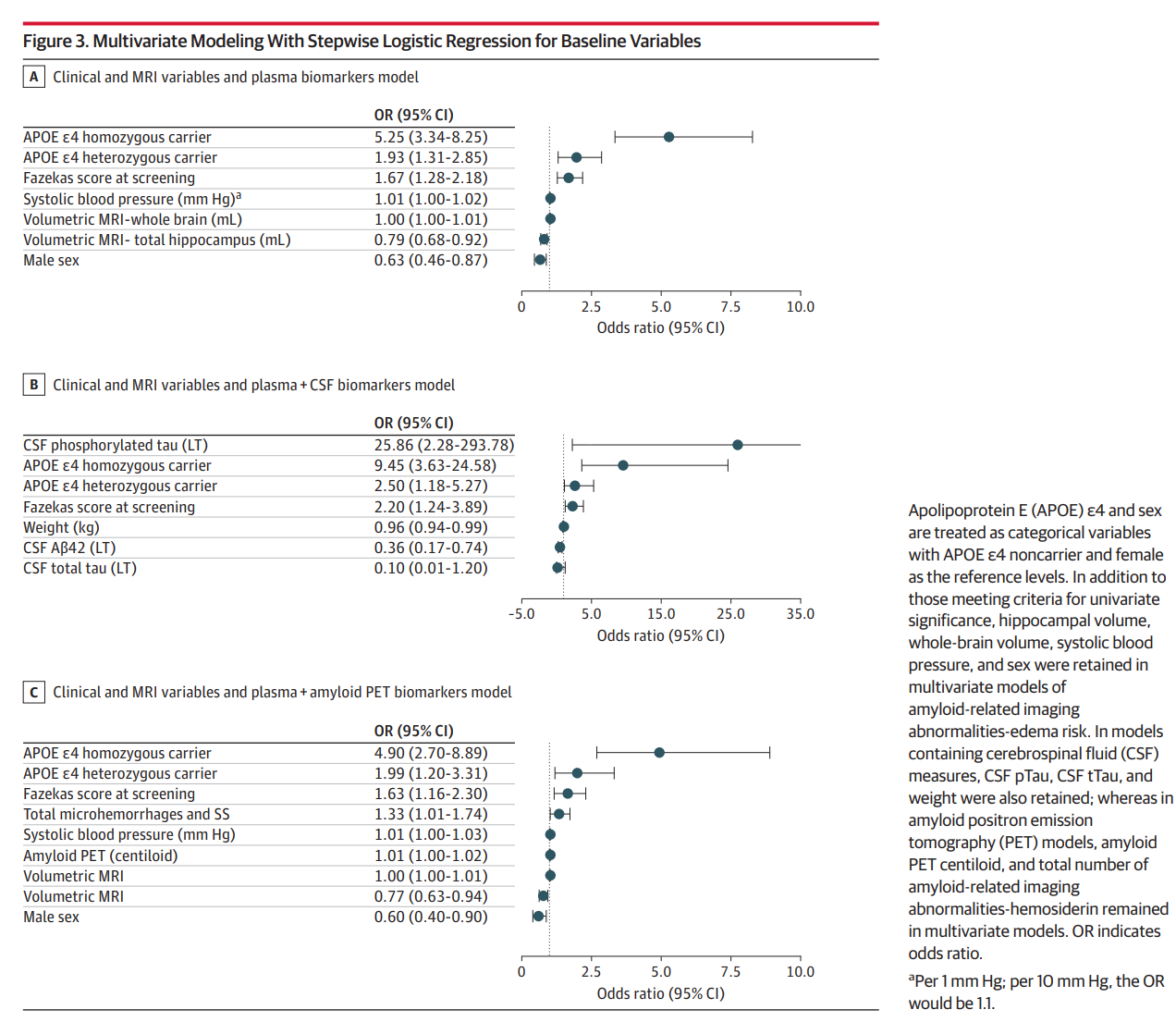
关键风险因素分析
| 风险因素 | ARIA-E风险(单变量) | 多变量模型中OR(95% CI) |
|---|---|---|
| APOE ε4纯合子 | HR=4.65 (3.23-6.70), p<0.001 | 4.90 (2.70-8.89) |
| APOE ε4异合子 | HR=1.98 (1.40-2.80), p<0.001 | 1.99 (1.20-3.31) |
| 脑白质高信号(Fazekas) | HR=1.65 (1.32-2.05), p<0.001 | 1.63 (1.16-2.30) |
| CSF Aβ42浓度(降低) | HR=0.40 (0.25-0.65), p<0.001 | 0.36 (0.17-0.74) |
| 微出血和表层铁沉积数目 | HR=1.31 (1.12-1.53), p=0.001 | 1.33 (1.01-1.74) |
| 收缩压(每1毫米汞柱) | 较弱相关 | 1.01 (1.00-1.03) |
| 体重 | — | 0.96 (0.94-0.99) |
-
ARIA的长期影响
采用认知和功能量表(CDR-SB、ADAS-Cog13、ADCS-ADL、FAQ)评估,结果显示ARIA-E事件对长期认知功能及日常生活能力无显著负面影响。无论是否发生ARIA-E,调整后的临床表现均无统计学差异,支持ARIA-E多为可逆且无持久认知损害。 -
ARIA复发与治疗管理
ARIA-E复发率较高,尤其在APOE ε4纯合子中更明显。68%的复发ARIA-E事件影像学评分与首次相当,症状学表现亦无明显加重。ARIA发生后,根据BGTS评分实施剂量暂停和调整,及时监测是确保安全的关键。
研究价值与临床意义
本研究系统揭示了更汀芦单抗治疗早期AD患者ARIA尤其是ARIA-E的风险因子及病程特征,丰富了对抗Aβ单抗治疗安全性的认知。APOE ε4基因剂量效应,伴随脑血管共病(微出血、白质病变)和较重Aβ病理,明显提升ARIA-E风险,提示血管病理对ARI A的发生有重要促发作用。这些因素反映了可能的共同病理基础,如脑淀粉样血管病(CAA)等,加深了对ARIA发生机制的理解。ARIA虽然较常见,但多无症状或轻症,且对认知功能无长期负面影响,支持合理监测下的安全管理策略。此外,研究总结的风险特征支持临床中开展个体化风险评估,制定差异化随访计划,有助于提升抗Aβ单抗临床应用时的患者安全。
值得注意的是,更汀芦单抗首次ARIA-E多于治疗一年内出现,但偶有晚发事件,提示临床需长期警惕ARIA发生。严密神经影像学监测和症状管理是保障患者安全的关键。此外,本研究也是首个详细披露多例严重症状性ARIA-E病例,有助于临床医生识别该不良事件的表现与应对,特别是避免误诊为脑卒中而错误用药。
梅斯编辑点评
本研究凭借GRADUATE I/II及PostGraduate试验的庞大数据量,首次系统揭示早期AD抗Aβ单抗更汀芦单抗相关ARIA发生的多维度风险因素及其临床结局,为抗淀粉样蛋白疗法的安全管理提供了有力证据。APOE ε4剂量效应已知,这项研究进一步明确脑血管共病与AD蛋白病理的协同作用,提示未来应加大对脑血管影像学指标及生物标志物的研究,优化风险评估模型。
未来研究方向包括:1)针对不同靶点和结构的抗Aβ药物,验证这些风险因素是否通用,以指导不同治疗方案的安全设计;2)深入阐明ARIA发生机制,探索预防和早期干预策略;3)开发敏感性更高的影像和生物标志物,实现ARIA的精准预测和动态监测;4)对严重ARIA事件的临床应对策略进行规范,制定再治疗指导原则。
随着新一代抗体药物(如正在研发的脑穿透性强化型单抗)进入临床,ARIA的发生模式和风险特征可能发生改变,定期回顾和更新安全管理指南显得尤为必要。
原始出处:
Salloway S, Wojtowicz J, Voyle N, Lane CA, Klein G, Lyons M, Rossomanno S, Mazzo F, Bullain S, Barkhof F, Bittner T, Schneider A, Grundman M, Aldea R, Boada M, Smith J, Doody R. Amyloid-Related Imaging Abnormalities (ARIA) in Clinical Trials of Gantenerumab in Early Alzheimer Disease. JAMA Neurol. 2025 Jan 1;82(1):19-29. doi: 10.1001/jamaneurol.2024.3937. Erratum in: JAMA Neurol. 2025 Feb 24. doi: 10.1001/jamaneurol.2025.0076. PMID: 39556389; PMCID: PMC11574721.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#阿尔茨海默病# #更汀芦单抗#
21 举报