Sci Adv:中山大学毛铎等团队合作报道脂滴富集型发光团实现巨噬细胞过继转移治疗细菌性脓毒症
2025-06-11 iNature iNature 发表于上海
该研究报道了一种新型发光小分子TPA2PyPh的强效抗菌特性及其在脂滴工程化巨噬细胞移植策略治疗细菌性脓毒症中的应用潜力。
细菌性脓毒症是一种危及生命的全身性感染炎症反应,全球每年累及超过3000万患者,其临床预后因抗生素耐药性和免疫抑制状态而显著恶化。
2025年6月6日,中山大学毛铎和新加坡国立大学刘斌共同通讯在Science Advances在线发表题为“Lipid droplet–enriched luminogens enable adoptive macrophage transfer for treatment of bacterial sepsis”的研究论文。该研究报道了一种新型发光小分子TPA2PyPh的强效抗菌特性及其在脂滴工程化巨噬细胞移植策略治疗细菌性脓毒症中的应用潜力。
通过将TPA2PyPh与巨噬细胞直接共孵育构建的工程化巨噬细胞,可使该发光体精确结合于细胞内脂滴结构。当吞噬病原菌时,负载TPA2PyPh的巨噬细胞能利用天然脂质摄取机制将发光分子递送至胞内细菌,通过破坏细菌膜结构并插入细菌DNA,从而实现病原体清除。研究数据显示,过继移植TPA2PyPh负载的巨噬细胞可显著降低脓毒症模型小鼠的细菌负荷,并使死亡率大幅下降。本研究表明TPA2PyPh作为一种高效抗菌剂的治疗潜力,同时验证了过继性脂滴工程化巨噬细胞移植策略在脓毒症及重症感染性疾病治疗中的临床应用价值。

细菌性脓毒症是一种危及生命的临床生化综合征,其特征是机体对微生物侵袭的异常反应导致急性器官功能障碍。作为全球主要致死原因,该病每年约造成4890万新发病例和110万死亡病例,对国际医疗体系构成重大挑战。根据临床指南,抗生素治疗仍是脓毒症治疗的基石。然而,抗生素耐药性的日益普遍使得有效抗生素的选择愈加困难,为脓毒症的成功治疗设置了重大障碍。临床观察表明,尽管超过60%的脓毒症患者在急性炎症期初期存活,但会迅速进展至长期免疫抑制状态,其特征为免疫细胞功能障碍和细胞凋亡,导致免疫功能瘫痪,从而削弱清除入侵病原体及继发细菌感染的能力。因此,针对细菌性脓毒症的替代治疗策略开发正受到越来越多的关注,这种策略应通过非抗生素途径清除入侵病原体,同时重建免疫系统以应对脓毒症后免疫抑制,从而实现对该病的全面治愈。
过去数十年间,研究者们致力于寻找缓解感染所致免疫失调的潜在治疗靶点,例如调控过氧化氢(H₂O₂)、超氧阴离子(O₂·⁻)和羟基自由基(·OH)等活性氧簇(ROS),以及靶向过敏毒素C5a。但这些方法面临疗效不稳定、成本高昂和给药复杂等挑战。近年来,过继性细胞转移(ACT)已成为治疗严重细菌性脓毒症伴免疫抑制患者的有效手段。该技术通过筛选患者或供体来源的免疫细胞进行基因修饰以增强其抗感染能力,既能直接清除病原体,又可调节炎性细胞因子产生以防止组织损伤,还能恢复免疫系统平衡以对抗脓毒症常见的免疫抑制状态。
目前脓毒症ACT治疗最常用的细胞包括工程化T细胞、巨噬细胞、自然杀伤细胞和树突状细胞。其中,巨噬细胞因其卓越的细菌吞噬能力及同时激活先天免疫和适应性免疫系统的特性,成为理想的抗菌治疗细胞。已有多种过继性工程巨噬细胞策略被开发,主要通过纳米技术强化溶酶体相关抗菌机制,从而实现细胞输注后的有效细菌清除。但现有溶酶体工程化ACT策略存在明显缺陷:包括金黄色葡萄球菌和大肠杆菌在内的多种细菌已进化出免疫逃逸策略以躲避吞噬溶酶体杀伤,导致其在胞内存活并引发反复感染。因此,亟需开发新型抗菌制剂以克服免疫逃逸,提高ACT治疗脓毒症的疗效。
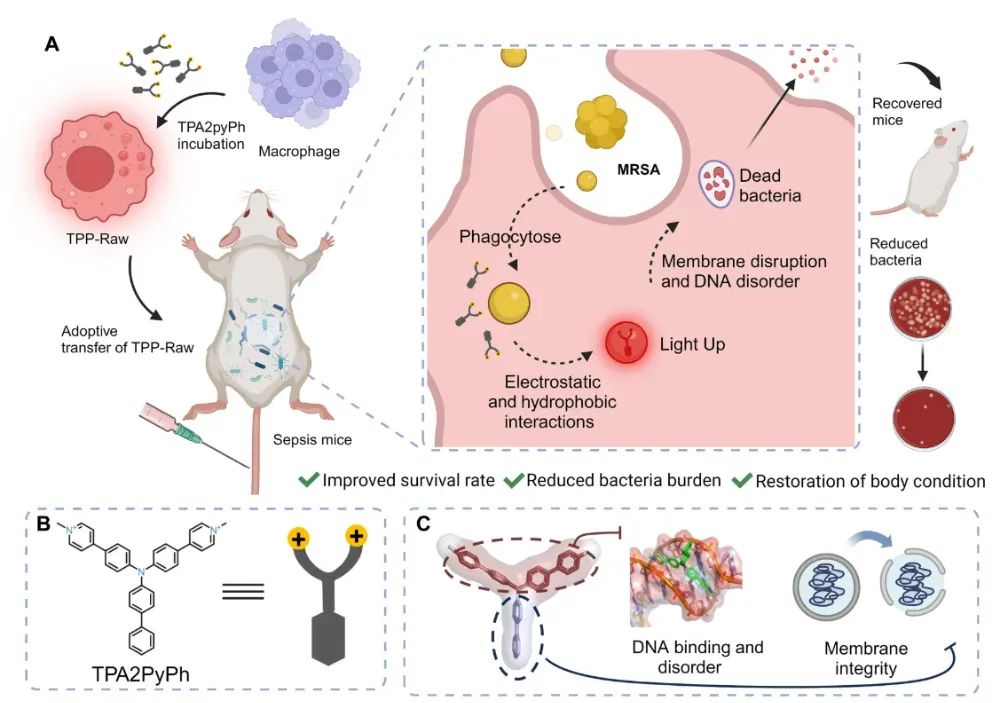
模式流程图(图片源自Science Advances)
最新研究发现,脂滴(LDs)是真核细胞中整合细胞代谢与宿主防御的先天免疫枢纽。LDs不仅储存着生成信号分子、膜结构组件和代谢能量所需的必需脂质,还可作为营养源吸引寄生虫、细菌和病毒等胞内病原体,这揭示了LDs超越代谢功能的先天免疫潜能。基于这些发现,作者提出可将LDs作为ACT过程中递送治疗药物的潜在靶点,利用其在免疫功能与病原体互作中的关键作用。为实现LD介导的抗菌功能,需要兼具优异LD靶向效应和强效杀菌能力的抗菌剂,以促进抗菌物质与LDs高效结合及相应细菌的捕获杀灭。当前LD靶向分子的设计范式通常通过构建具有显著亲脂性的化合物,使其有效整合至富脂环境。该策略已推动多种LD靶向荧光探针(如BODIPY衍生物和油红O)的开发,这些探针被广泛用于追踪胞内LDs。因此,若能为这些荧光探针进一步功能化修饰特定基团,则有望实现LD相关病原体的同步靶向与杀灭。
本研究设计合成了发光化合物TPA2PyPh,其具有高疏水性和刚性的联苯单元,可有效穿透细胞膜并后续负载至巨噬细胞LDs中。此外,TPA2PyPh具有强效杀菌活性,能高效插入双链DNA(dsDNA)沟槽并继发诱导细菌DNA断裂。将TPA2PyPh标记的巨噬细胞(TPP-巨噬细胞)注射至耐多药细菌诱导的脓毒症小鼠体内后,TPP-巨噬细胞可主动捕获并吞噬入侵细菌,随后通过天然脂质摄取机制将LD负载的TPA2PyPh递送至胞内细菌,进一步破坏细菌膜完整性并诱导DNA紊乱以实现杀菌。体内实验证实,这种过继性TPP-巨噬细胞策略能有效清除小鼠腹腔和血液中的细菌,同时改善体内免疫抑制微环境,成功挽救细菌性脓毒症小鼠。这种LD工程化抗菌策略通过强化宿主防御机制,实现了脓毒症中耐多药细菌的高效清除。
原文链接:
https://www.science.org/doi/10.1126/sciadv.adt8376
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#Nat#哇
19 举报
#巨噬细胞# #细菌性脓毒症#
22 举报