JEV:天津医科大学岳丹等团队发现PDCD10调节囊泡运输并促进透明细胞肾细胞癌的进展
2025-07-15 iNature iNature 发表于上海
该研究强调了程序性细胞死亡蛋白 10(PDCD10) 作为ccRCC中囊泡运输调控因子的重要性,以及开发新型抗癌疗法的潜在靶点。
囊泡运输是细胞中一个至关重要的过程,在肿瘤进展中发挥着重要作用。
2025年6月25日,天津医科大学岳丹、王勇和天津大学陈瑞冰共同通讯在Journal of Extracellular Vesicles在线发表题为“Programmed Cell Death Protein 10(PDCD10) Regulates Vesicle Trafficking and Contributes to the Progression of Clear Cell Renal Cell Carcinoma”的研究论文。该研究强调了程序性细胞死亡蛋白 10(PDCD10) 作为ccRCC中囊泡运输调控因子的重要性,以及开发新型抗癌疗法的潜在靶点。
对50个透明细胞肾细胞癌(ccRCC)肿瘤样本进行了全面的转录组学和蛋白质组学分析,数据系统地描绘了分子图谱的变化。有趣的是,我们的研究发现了囊泡运输过程的严重失调。特别是PDCD10在ccRCC中过表达,功能分析表明PDCD10在体外促进细胞增殖、迁移和侵袭,并在体内增强肿瘤生长。此外,我们还发现PDCD10是内吞作用和外泌体分泌的关键调控因子。细胞外囊泡(EVs)的蛋白质组学分析表明,PDCD10的过表达改变了EVs中的货物含量,并增加了细胞粘附和细胞外基质分子的丰度。此外,厄洛替尼治疗可抑制PDCD10诱导的内吞作用,并抑制细胞增殖和侵袭。

肾细胞癌 (RCC) 是全球第三大泌尿系统癌症,也是泌尿系统癌症死亡的主要原因。RCC起源于肾小管上皮细胞,可分为透明细胞肾细胞癌 (ccRCC)、乳头状肾细胞癌和嫌色细胞肾细胞癌。最常见的RCC亚型是ccRCC,约占RCC的 75%。ccRCC 通常对化疗和放疗均具有耐药性,且手术干预后高复发率和转移率是其不良预后的重要原因。深入了解ccRCC的分子机制对于开发新的治疗策略以改善ccRCC患者的生存结局至关重要。
囊泡运输作为细胞的基本过程,在细胞间通讯和其他各种生理功能中发挥着至关重要的作用。囊泡运输各种分子,例如离子、代谢物、RNA、脂质和蛋白质,协调细胞内和细胞间必需物质的运输和交换。细胞外囊泡 (EV) 的含量可能反映了来自母细胞的细胞质成分的被动掺入,而EV中的某些生物分子涉及高度调控的货物分选机制,这由不同生理和病理条件下细胞类型特异性的蛋白质特征所证明。超过 10% 的人类基因组编码了参与膜和囊泡运输的蛋白质;因此,囊泡运输失调与多种疾病的发病机制有关,包括癌症。囊泡运输包含多个协调的过程,包括细胞内运输(例如胞吞和胞吐)、自噬介导的货物运输以及细胞器间膜接触动力学(例如内质网-线粒体相互作用),这些过程共同促进生物分子在细胞内和细胞间的移动和运输。越来越多的证据表明,囊泡运输在驱动肿瘤发生发展的各种生物学机制中发挥着至关重要的作用,例如增殖、迁移、侵袭和细胞代谢。囊泡可以将旁分泌介质、血管生成因子和生长因子受体(例如 VEGF、CXCR4 和 HER2)运输至靶细胞。
胞外囊泡 (EVs) 在肾脏生理学中发挥着至关重要的作用,其功能涵盖从肾脏发育的初始阶段到各种肾脏疾病的发病机制,包括急性肾损伤 (AKI)、慢性肾脏病 (CKD) 和肾细胞癌 (RCC)。在RCC中,EVs 通过 VHL/HIF/VEGF 通路和 miRNA(例如 miR-92a)促进血管生成,这可能会降低酪氨酸激酶抑制剂 (TKI) 等抗血管生成疗法的疗效。 EVs通过抑制树突状细胞成熟、使巨噬细胞极化为免疫抑制性M2表型以及通过PD-L1或miRNA介导的机制间接抑制T细胞功能,促进肿瘤免疫逃逸。此外,EVs还通过重塑转移前微环境、激活上皮-间质转化 (EMT) 以及通过AZU1等货物蛋白增强血管通透性,从而促进转移进展。此外,囊泡通过转移STAT3和lncRNA(例如IGFL2-AS1)等分子,介导靶向治疗(例如舒尼替尼)的耐药性,也可能促成免疫疗法耐药性。这些多方面的作用凸显了囊泡作为肾细胞癌进展的关键介质的作用。然而,控制肾细胞癌囊泡运输过程的基本分子机制和关键因素仍然很大程度上尚不清楚。
程序性细胞死亡蛋白 10(PDCD10) 最初被认为是一种凋亡相关蛋白。PDCD10蛋白的功能主要位于两个区域:N端二聚化结构域,用于PDCD10同源二聚化或与生发中心激酶 III (GCKIII) 相互作用;C端黏着斑靶向 (FAT) 同源结构域,用于与CCM2、纹状体等相互作用。PDCD10已被发现定位于多个亚细胞区室,例如细胞质、高尔基体和质膜。近期研究表明,PDCD10作为一种衔接蛋白,在细胞存活、迁移、细胞分化、囊泡运输和细胞衰老等多种生物学过程中发挥着多重作用。此外,PDCD10的异常表达或突变在癌症中很常见,并且可能根据癌症类型发挥不同的生物学功能。据报道,PDCD10在胶质瘤、乳腺癌和前列腺癌中表现出促肿瘤作用,并在脑膜瘤和结直肠癌中表现出抗肿瘤作用。这种双重功能可能归因于PDCD10的组织特异性,它与不同组织中不同细胞伙伴的相互作用决定了其最终的生物学结果。此外,Pdcd10调控培养小鼠集合管细胞中的囊泡运输,并通过调节Aqp2膜靶向作用影响顶端细胞的胞内囊泡运输。此外,Pdcd10还能增强Caveolin-1介导的内吞作用,增加 Caveolae 的形成,从而促进周细胞与内皮细胞分离,促进脑微血管内皮细胞中脑海绵状血管瘤 (CCM) 的形成。然而,PDCD10在肾细胞癌 (RCC) 中的作用尚待探索。
本研究首先对 50 例ccRCC肿瘤样本进行了转录组学和蛋白质组学整合分析。基于这些数据,我们能够绘制出ccRCC中囊泡运输失调的网络。有趣的是,我们观察到PDCD10在ccRCC肿瘤样本中在蛋白质水平上过表达,并通过免疫组织化学进一步验证了其过表达。功能分析表明,PDCD10在体外促进ccRCC细胞的增殖、迁移和侵袭,并在体内促进肿瘤生长。此外,我们还发现PDCD10是ccRCC细胞内吞作用和EV分泌的关键调控因子。基于EV的蛋白质组学分析,我们发现ccRCC细胞中PDCD10的过表达改变了EV中的货物含量。此外,我们的研究表明,厄洛替尼可抑制PDCD10过表达增强的ccRCC细胞迁移和侵袭能力,从而确立PDCD10是开发新型抗癌疗法的潜在靶点。
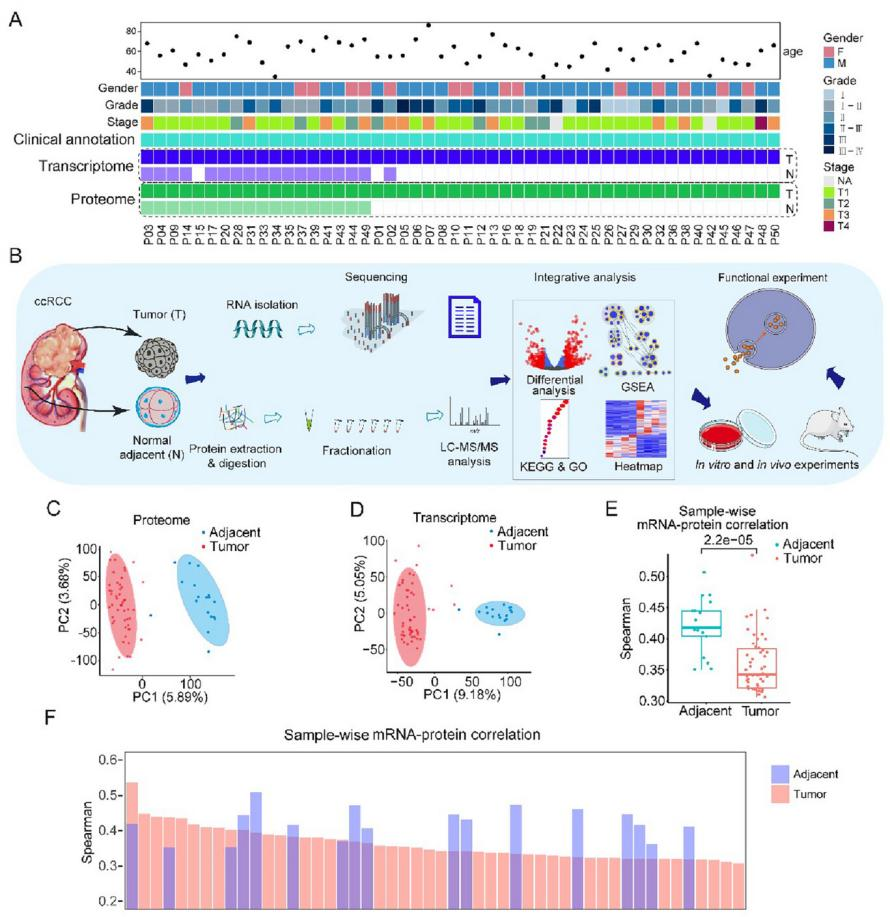
图1 ccRCC 肿瘤和配对相邻非肿瘤组织样本的转录组学和蛋白质组学分析(图源自JEV)
原文链接:
https://isevjournals.onlinelibrary.wiley.com/doi/10.1002/jev2.70108
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#透明细胞肾细胞癌# #囊泡运输#
2 举报