Nat Commun:南京中医药大学王若宁研究开发了一种用于治疗异质性和免疫抑制性恶性肿瘤的纳米疫苗
2025-06-09 iNature iNature 发表于上海
研究开发纳米疫苗 nAg-MRDE/Mn,结合新抗原与原位疫苗,通过激活先天免疫、调节巨噬细胞表型重塑肿瘤微环境,增强特异性免疫,抑制肿瘤生长及术后复发,为个性化免疫治疗提供思路。
新抗原(nAg)疫苗可以诱导抗肿瘤特异性免疫,肿瘤杀伤促进抗原进一步扩散,有望改善预后。然而,在疫苗的选择压力下癌细胞的突变和免疫抑制的肿瘤微环境使得治疗效果不尽如人意。
2025年5月31日,南京中医药大学药学院王若宁唯一通讯在Nature Communications上在线发表题为“Neoantigens combined with in situ cancer vaccination induce personalized immunity and reshape the tumor microenvironment”的研究论文。研究开发了一种纳米疫苗(nAg-MRDE/Mn),它可以递送nAg并诱导原位癌症疫苗接种,通过调节免疫抑制细胞和激活先天免疫反应来协同促进个性化免疫反应,增强抗原扩散并改善微环境。
实验表明,nAgs由树突状细胞呈递,由T细胞表达,T细胞配合原位疫苗接种刺激特异性免疫。参与免疫抑制的细胞,如M2巨噬细胞和调节性T细胞下调,而M1巨噬细胞和自然杀伤细胞增加。此外,载有趋化因子和nAg-MRDE/Mn的水凝胶抑制术后肿瘤复发,nAg-MRDE/Mn和αPD-1的组合提高了αPD-1的治疗效果。本研究验证了该策略的临床潜力,并为改进新抗原疫苗提供了思路。

免疫疗法改变了癌症管理,但肿瘤异质性和免疫冷表型限制了许多患者的长期肿瘤抑制。基于新抗原的个性化肿瘤疫苗可富集肿瘤特异性T细胞的内源性库,以响应肿瘤异质性。然而,迄今为止的临床试验尚未广泛验证其疗效,因为缺乏新抗原表达的肿瘤细胞在选择压力下增殖,产生多种新型表位突变。目前的策略是通过设计针对多种新抗原的癌症疫苗来降低免疫逃逸的可能性。值得注意的是,两项阳性临床试验(NCT03897881,NCT04161755)联合免疫检查点抑制(ICI)疗法,进一步研究认识到这可能是因为ICI疗法使T细胞更容易被垂死的肿瘤细胞释放的新抗原和肿瘤相关抗原(TAA)激活,从而导致额外的肿瘤定向免疫反应,称为表位扩散。这种抗肿瘤T细胞库的扩展通常预示着良好的预后和较长的无进展生存期。不幸的是,这种程度的表位扩散在初始获益后仍然可以进行免疫逃逸。因此,需要有效促进抗原扩散的策略。此外,最近的研究推测,新抗原联合免疫原性细胞死亡(ICD)是肿瘤微环境(TME)的潜在治疗策略,其中免疫治疗选择因免疫沙漠表型而受到限制。受此启发,研究提出新抗原和原位癌症疫苗接种的结合可以帮助克服由肿瘤异质性引起的免疫逃逸。
TME中的免疫抑制机制不仅影响肿瘤免疫治疗的疗效,还会阻碍自然免疫反应。值得注意的是,免疫抑制TME中肿瘤炎症的增加和免疫反应的刺激可以促进冷肿瘤向热肿瘤的转化。增加T细胞的频率和中和免疫抑制细胞可以通过重编程免疫抑制TME进一步促进寒冷肿瘤的逆转。值得注意的是,癌细胞中环GMP-AMP合酶-干扰素基因刺激因子(cGAS-STING)通路的激活有助于I型干扰素的产生,从而增强自然杀伤(NK)细胞活性。这有助于确保抗原的交叉呈递以激活适应性免疫,并进一步靶向具有抗原漂移的异质性肿瘤。
研究展示了一种由STING激动剂(Mn2+),树突状细胞来源的外泌体(DEs)和杂合肽α-Mel- nAg组成的纳米疫苗(nAg- mrde /Mn),该杂合肽整合了靶向肽(仿生肽D4F),穿孔肽(Mel)和nAg。nAg可被模型新抗原卵清蛋白(OVA)替代。根据治疗要求,可将nAg-MRDE/Mn装入含有CXCL10的ros响应性水凝胶(TSPBA-PVA)中。这种基因工程修饰使nAg-MRDE/Mn能够通过多种途径协同靶向肿瘤。体外和体内研究表明,通过cGAS-STING通路,新抗原得到有效交叉提呈,肿瘤细胞的ICD效应物被激活,NK细胞被激活,TME得到改善。新抗原与原肿瘤疫苗结合后,抗肿瘤特异性免疫水平有一定提高。对负载疫苗的水凝胶术后治疗以及疫苗在其他异质性肿瘤如肺癌脑转移和三阴性乳腺癌中的适用性进行了探索。αPD-1联合治疗提高了对免疫检查点抑制的应答率。通过模拟临床条件探索疫苗的转化潜力。综上所述,本研究开发了一种用于治疗异质性和免疫抑制性恶性肿瘤的纳米疫苗,为加强新抗原疫苗的个性化免疫治疗提供了一些思路。
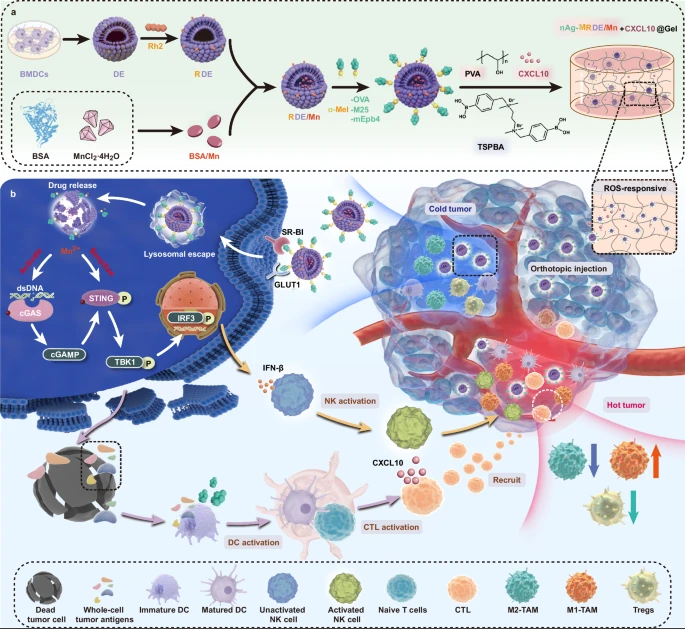
图1制备nAg-MRDE/Mn + CXCL10@Gel及抗肿瘤免疫反应的过程。(摘自Nature Communications)
参考消息:
https://doi.org/10.1038/s41467-025-60448-3
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#肿瘤微环境# #纳米疫苗#
28 举报