STTT:四川大学郑莉等团队研究调查了onatasertib联合特瑞普利单抗治疗晚期实体瘤患者的安全性、耐受性和有效性
2025-07-01 iNature iNature 发表于上海
研究者进行了一项临床试验(NCT04337463)来研究mTORC1/2抑制剂onatasertib与PD-1抗体特瑞普利单抗联合治疗晚期实体瘤患者的疗效和安全性。
临床前研究表明,mTORC1/2抑制剂与PD-1抗体的组合对实体瘤表现出协同作用。然而,尚未报告支持这种联合治疗的临床数据。
2025年6月25日,四川大学华西医院郑莉、德琪医药有限公司谢辉共同通讯在Signal Transduction and Targeted Therapy上在线发表题为“Multicenter phase 1/2 study of onatasertib, a dual TORC1/2 inhibitor, combined with the PD-1 antibody toripalimab in advanced solid tumors”的研究论文。研究者进行了一项临床试验(NCT04337463)来研究mTORC1/2抑制剂onatasertib与PD-1抗体特瑞普利单抗联合治疗晚期实体瘤患者的疗效和安全性。
这项开放标签的1/2期临床试验包括剂量递增和剂量扩展队列,以评估安全性、耐受性、客观缓解率(ORR)、疾病控制率(DCR)和无进展生存期(PFS)。共有46例患者入组,接受剂量为15mg、20mg或30mg每日一次(QD)的onatasertib,联合特瑞普利单抗240mg每3周一次(Q3W)。未观察到剂量限制性毒性,最常见的3级或4级治疗紧急不良事件是淋巴细胞减少(23.9%)和皮疹(19.6%)。总体ORR为26.1%,DCR为73.9%,中位PFS为4.3个月。在宫颈癌患者中,无论PD-L1表达如何,ORR均为52.4%,DCR为90.5%,中位PFS为5.8个月。值得注意的是,15mg联合剂量的中位PFS为7.8个月。总之,onatasertib联合特瑞普利单抗的安全性是可控的,并且在晚期实体瘤中显示出令人鼓舞的临床活性,尤其是在宫颈癌患者中,无论PD-L1表达如何。该组合的推荐2期剂量确定为onatasertib15mgQD和特瑞普利单抗240mgQ3W。

免疫检查点抑制剂(CPI)对各种实体瘤恶性肿瘤的治疗结果产生了显著影响。然而,只有一部分患者获得了长期治疗益处。因此,需要涉及多种抗肿瘤机制的新型有效疗法来增强基于PD-1/L1的免疫疗法的疗效。临床前研究表明,mTOR抑制剂与PD-1抗体联合使用对多种肿瘤类型具有协同作用。因此,有充分的理由将这两种治疗方式结合起来,以改善和延长晚期癌症患者的抗肿瘤反应。
雷帕霉素靶蛋白(mTOR)是一种高度保守的丝氨酸/苏氨酸激酶,作为细胞生长的核心调节因子发挥作用,整合来自有丝分裂原、能量和营养的信号。它位于磷脂酰肌醇 3 激酶(PI3K)-蛋白激酶 B(AKT)通路的下游,并通过两个不同的复合物 mTORC1 和 mTORC2 来执行其生物学功能。在许多癌症中,PI3K-AKT-mTOR 通路的异常激活在癌细胞增殖和存活中起着关键作用。在肾细胞癌(RCC)中,据报道mTOR通路在特定细胞条件下调节缺氧诱导因子(HIF)蛋白表达。在大多数透明细胞RCC病例中观察到的vonHippel-Lindau(VHL)基因双等位基因突变引起的HIF-1α和HIF-2α的不适当积累,被认为是RCC肿瘤发生的关键步骤。神经内分泌肿瘤(NETs)与一些罕见的家族综合征有关,这些综合征是由与PI3K-AKT-mTOR通路相关的基因突变引起的。一些发现表明PI3K-AKT-mTOR通路代表了经典的治疗靶点,mTOR抑制剂目前正在开发为各种癌症的潜在治疗药物。
第一代变构(非竞争性)mTOR抑制剂,专门靶向mTORC1,已被批准用于治疗晚期RCC。此外,依维莫司已获准用于治疗HER2阴性乳腺癌、室管膜下巨细胞星形细胞瘤(SEGA)以及进行性或转移性胰腺、胃肠道和肺NETs。然而,第一代 mTOR 抑制剂由于仅针对mTORC1,存在一定的局限性,这会导致 AKT 的反馈激活,并对 mTORC2产生耐药性。第二代ATP竞争性 mTOR 抑制剂能够同时抑制 mTORC1 和 mTORC2,从而克服了仅使用mTORC1抑制剂时出现的反馈抑制现象。此外,第二代 mTOR 抑制剂已被报道具有更强的效力和选择性。这些抑制剂中的一些除了抑制 mTORC1和mTORC2外,还针对 PI3K。除了直接的肿瘤抑制作用外,第一代和第二代 mTOR 抑制剂均被报道可调节免疫。
Onatasertib(也称为ATG-008或CC-223)是一种靶向mTORC1和mTORC2的选择性mTOR激酶抑制剂,已对肝细胞癌、神经内分泌肿瘤和其他肿瘤类型显示出抑制作用。它表现出可接受且可管理的安全性,最大耐受剂量为每日一次(QD)45 毫克。由于其独特而广泛的mTORC1/2抑制特性、调节TME的能力和直接的抗肿瘤活性,onatasertib被认为是免疫治疗联合治疗的合适候选者。
特瑞普利单抗是一种对人PD-1具有特异性的人源化IgG4κ单克隆抗体,已在中国获得国家药品监督管理局(NMPA)批准用作黑色素瘤、晚期鼻咽癌和转移性尿路上皮癌的单药治疗,并已获得美国食品药品监督管理局(FDA)批准用于治疗鼻咽癌。来自实体瘤患者的临床数据表明,特瑞普利单抗通常耐受性良好,批准剂量为240mg,静脉注射,每三周(Q3W)。值得注意的是,先前没有临床研究报道TORC1/2抑制剂与免疫检查点抑制剂的组合。在这里,研究介绍了TORCH-2研究的结果,这是一项非随机1/2期试验,调查了onatasertib联合特瑞普利单抗治疗晚期实体瘤患者的安全性、耐受性和有效性。
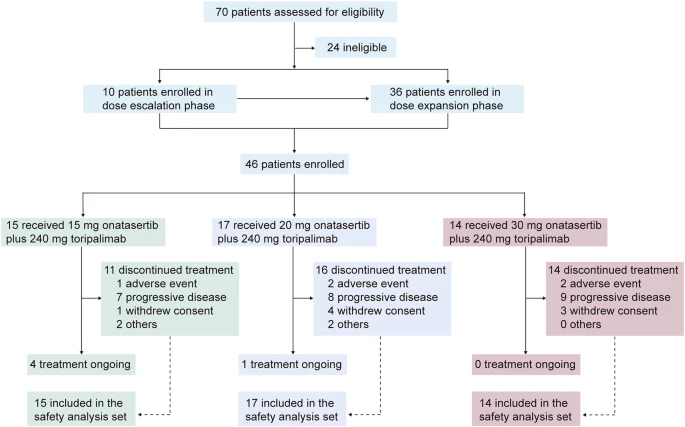
图1研究流程图(摘自Signal Transduction and Targeted Therapy)
参考消息:
https://doi.org/10.1038/s41392-025-02281-0
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#实体瘤# #特瑞普利单抗#
30 举报