J Hematol Oncol:抗体-药物偶联体临床试验相关治疗性不良事件全面解析
2025-07-13 MedSci原创 MedSci原创 发表于上海
本研究系统总结了ADCs相关治疗性不良事件,显示无论是早期临床试验还是后期注册试验,绝大多数患者都会经历至少1级的毒性事件,近半数患者会出现≥3级严重不良事件。
抗体-药物偶联体(ADCs)通过将细胞毒性药物精确递送至肿瘤细胞,提高治疗指数并减少对正常组织的损伤,成为精准抗癌治疗的重要方向。截至目前,美国FDA已批准14款ADCs上市,近190款处于临床开发阶段。尽管ADCs在多项随机试验中显示优于传统化疗的疗效与安全性(如DESTINY-Breast06和TROPiCS-02试验),但其仍存在意外的、剂量限制性毒性,尤其是血液学、神经系统和眼科毒性问题。部分毒性可能源自ADC全身循环中的载药释放、正常组织的表达靶点所致的“非肿瘤靶向”毒性,或免疫反应等复杂机制。此外,不同ADCs构成中的靶点选择、连接子类型以及DAR(载药量)等因素对毒性谱也有较大影响。目前针对ADCs相关毒性的系统总结及结构功能关系解释尚属空白,有必要以真实世界和临床试验数据为支撑,系统揭示各种成分对具体不良事件的影响。

本文回顾性分析了2014年至2024年期间,英国皇家马斯登医院新药开发部门(DDU)中参与ADCs的131例第I期患者的治疗相关不良事件,并对比同期FDA批准的15个关键Ⅱ/Ⅲ期ADCs注册试验中共2666例患者的安全性数据。通过单因素及多因素逻辑回归,探究ADCs各结构组分如何影响毒性谱系,旨在为未来ADCs的设计、临床开发和用药管理提供科学依据。全文发表在Journal of Hematology & Oncology杂志上。
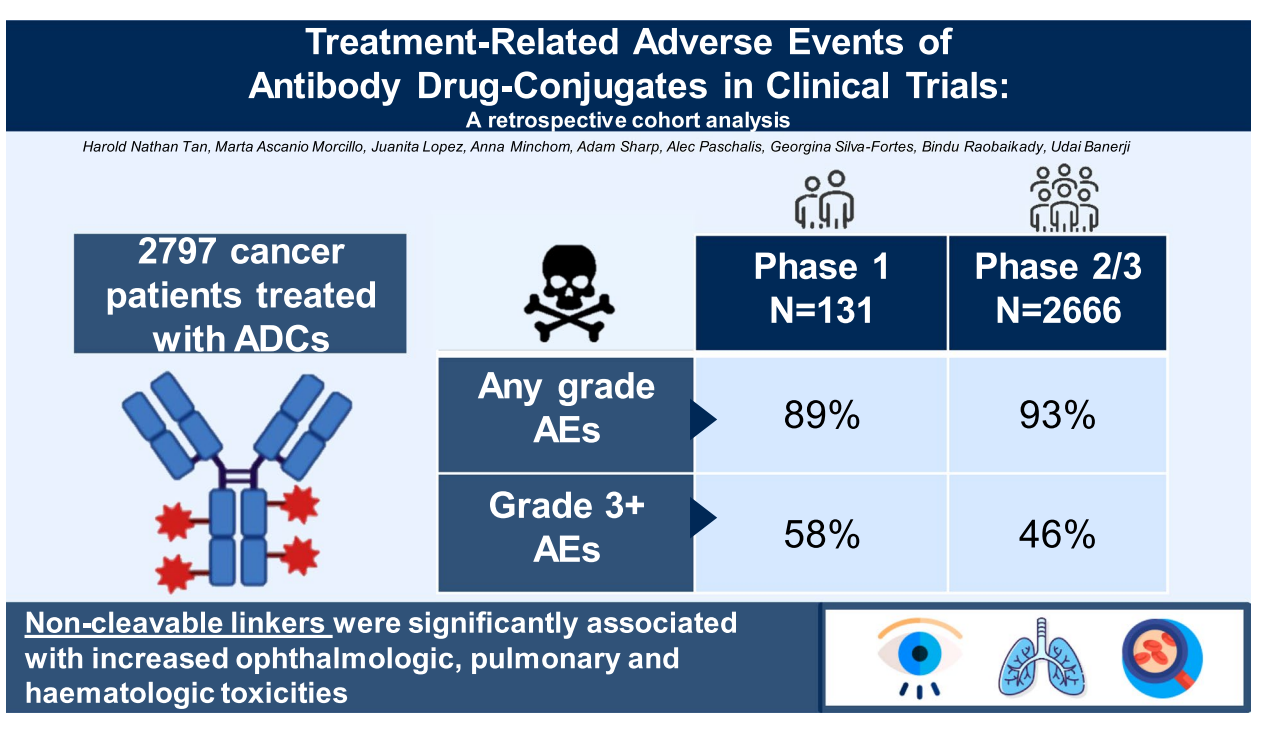
本研究采集了皇家马斯登DDU自2014年1月至2024年1月间参与ADCs治疗的第I期患者临床数据,使用NCI CTCAE v5.0标准评估不良事件,并与公开发表的FDA批准ADCs关键Ⅱ/Ⅲ期临床数据进行比较。对ADC组件(靶点类别、抗体亚型、连接子类别、载药类型、DAR)分别以单变量和多变量逻辑回归分析其与眼部、肺部、神经系统及血液学不良事件的相关性。采用R 4.4.1软件进行统计分析,以P<0.05为显著性阈值。
研究结果
1,基本患者特征
第I期队列n=131,主要实体瘤,女性占62%,以肺癌(20%)、乳腺癌(17%)及卵巢癌(15%)为主,绝大多数既往接受过≥3线化疗。
Ⅱ/Ⅲ期注册试验队列n=2666,女性比例67%,以HER2为主要靶点(32%),载药以微管结合剂为主(72%),大多数ADCs DAR集中于2-4,半数患者剂量超过3 mg/kg。
2,治疗相关不良事件概况
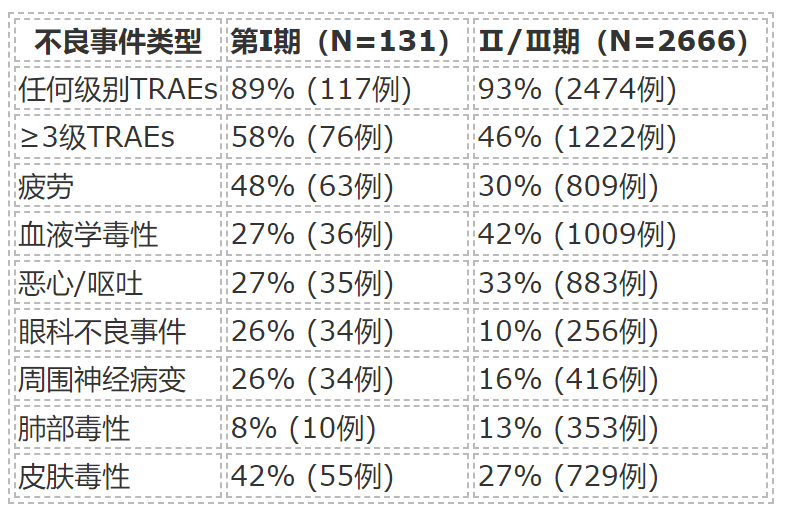
3,多变量分析统计关联
眼科毒性:唯一显著影响因素为“连接子类型”,非可裂解连接子增加眼部毒性风险(OR=1.45,P=0.01)。
肺部毒性:IgG1抗体(OR=107,P<0.001)、非可裂解连接子(OR=3.43,P<0.001)、DAR>4(OR=1.83,P=0.03)均与较高肺部不良事件风险相关;微管结合载药则显著降低肺部毒性风险(OR=0.14,P<0.001)。
血液学毒性:非可裂解连接子(OR=3.21,P<0.001)和DAR>4(OR=18.3,P<0.001)显著增加血液学不良事件风险。
神经病变:微管靶向载药物引发神经病变显著(OR=198,P<0.001);非血液学靶点(OR=0.65,P=0.002)及非可裂解连接子(OR=0.15,P<0.001)与神经病变风险降低相关。
讨论
本研究系统总结了ADCs相关治疗性不良事件,显示无论是早期临床试验还是后期注册试验,绝大多数患者都会经历至少1级的毒性事件,近半数患者会出现≥3级严重不良事件。早期第I期患者群体中疲劳及眼部毒性更为突出,可能因患者预后较差、治疗量递增而致;而晚期Ⅱ/Ⅲ期患者则血液学毒性较高,很大程度关联于血液肿瘤患者的纳入及持续治疗累积效应。
非可裂解连接子虽然提高血浆中的稳定性,理论上可减少非特异性载药释放,但其与眼部、肺部及血液系统毒性的高风险相关性挑战了这一认识,提示该类ADC在体内的代谢及局部递送机制可能导致载药物在眼角膜等敏感组织积聚,造成局部细胞损伤。以belantamab mafodotin为代表的ADC更验证了该关联。如果链接设计不佳,会发生包括“逆迈克尔反应”等非酶促药物脱离机制,导致眼部高度曝露及毒性。
微管靶向载药物如MMAE和MMAF与周围神经病变高度关联,反映了微管靶向化疗毒理学的延续性,这对与既往接受过其他神经毒性药物(如紫杉醇、顺铂)治疗的患者,进一步提升风险。
DAR的增加提供更高的单抗载药量以提高抗肿瘤效力,但与此同时也加剧了肺部和血液相关不良事件,反映了ADC整体药代动力学平衡的复杂性。DAR值的提升虽然带来潜在的疗效提升,但也应在ADC设计与临床应用中严格权衡,以期实现最佳的疗效-安全窗口。
本研究强调了ADCs设计各个组成部分之间存在复杂的相互作用影响毒性表现,未来应努力开发更稳定的连接子(如自水解型maleimide连接子)、更均一的载药方式(位点特异性偶联技术)以降低免疫原性及非靶向损伤。同时,探索非微管类新型载药物以减轻神经毒性,以及利用结构-功能关系来优化DAR以平衡效力与毒性,是未来ADCs研究的重点方向。
原始出处:
Tan et al. Treatment-related adverse events of antibody drug-conjugates in clinical trials. Journal of Hematology & Oncology. 2025;18:71. https://doi.org/10.1186/s13045-025-01720-3
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#抗体-药物偶联体#
6 举报
细胞毒性药物精确递送至肿瘤细胞,提高治疗指数并减少对正常组织的损伤
0 举报
抗体-药物偶联体(ADCs)通过将细胞毒性药物精确递送至肿瘤细胞,提高治疗指数并减少对正常组织的损伤,成为精准抗癌治疗的重要方向。
0 举报