肝癌患者存活时间再延长!《柳叶刀》:双免联合治疗或为一线治疗选择
2025-05-15 医学新视点 医学新视点 发表于上海
文章表示,研究结果支持纳武利尤单抗联合伊匹木单抗作为不可切除肝细胞癌一线治疗选择。
过去的5年间,不可切除肝细胞癌的治疗取得了一定的进展。PD-L1抑制剂阿替利珠单抗联合VEGF抑制剂贝伐珠单抗、CTLA-4抑制剂tremelimumab联合PD-L1抑制剂度伐利尤单抗等策略,相继成为不可切除肝细胞癌的一线治疗策略,用药后患者中位总生存期(OS)为16~19个月。在现有疗法的基础上,如何持续改善肝细胞癌患者长期预后,是临床持续探索的方向。
近日,《柳叶刀》(The Lancet)发表CheckMate 9DW试验预计划中期分析结果,表明在既往未接受治疗的不可切除肝细胞癌患者中,相比于TKIs单药治疗,PD-1抑制剂纳武利尤单抗联合CTLA-4抑制剂伊匹木单抗显著提高了中位OS(23.7个月 vs. 20.6个月),联合治疗使患者死亡风险降低了21%,未发现新的安全性问题。文章表示,研究结果支持纳武利尤单抗联合伊匹木单抗作为不可切除肝细胞癌一线治疗选择。

截图来源:The Lancet
CheckMate 9DW试验是开放标签、随机、3期临床试验,纳入2020年1月6日至2021年11月8日,全球25个国家和地区的163家医疗中心晚期肝细胞癌成人患者668例。所有患者均满足以下条件:1)既往均未接受过系统性治疗;2)至少有一处未治疗病灶;3)Child–Pugh评分为5分或6分;4)东部肿瘤协作组体能状态评分为0分或1分。
研究人员以1:1的随机比例分配患者接受以下任一治疗方式:
-
联合治疗组(335例):纳武利尤单抗(1 mg/kg)联合伊匹木单抗(3 mg/kg)治疗(每3周一次,最多4次),随后接受纳武利尤单抗单药(480 mg,每4周一次)治疗;
-
单药治疗组(333例):由研究者选择仑伐替尼(体重<60 kg,8 mg/d;体重≥60 kg,12 mg/d)或索拉非尼单药治疗(400 mg,每日2次);
截至2024年1月31日,联合治疗组和单药治疗组分别有133例(40%)和224例(69%)的患者因疾病进展而停止治疗。中位随访时间为35.2个月,相比于单药治疗组,联合治疗组中位OS显著提高(23.7个月 vs. 20.6个月,HR=0.79,95%CI:0.65~0.96,P=0.018)。第24个月时,联合治疗组和单药治疗组OS率分别为49%和39%;第36个月时,两组OS率分别为38%和24%。在不同年龄、不同性别的亚组中,联合治疗组的OS都优于单药治疗组。
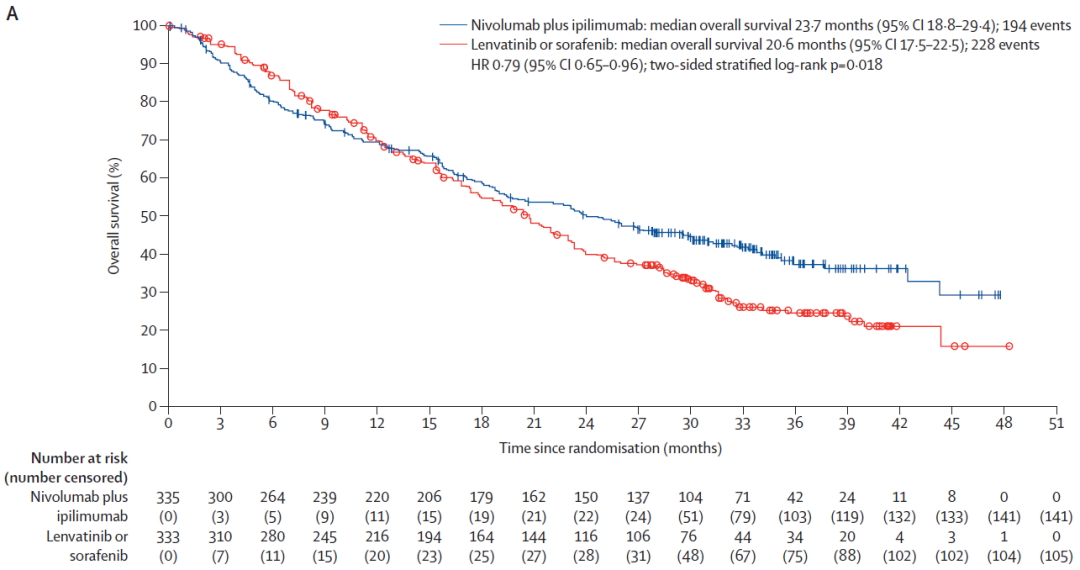
▲单药治疗组(红色)和联合治疗组(蓝色)OS对比(图片来源:参考文献[1])
从上图可观察到,两组OS曲线早期有交叉,但随后两组曲线持续分离,且联合治疗组明显更具优势。两组生存曲线早期交叉的可能原因较多,如与研究无关的不良事件引起的死亡率不平衡、肿瘤免疫治疗可能存在延迟效应,而靶向治疗对肿瘤的生长和进展影响更为直接等。因此,对于既往未接受过系统性治疗的不可切除肝细胞癌患者,纳武利尤单抗联合伊匹木单抗可带来长期获益。
联合治疗组确认的客观缓解率(ORR)也优于单药治疗组(36% vs. 13%,P<0.0001)。联合治疗组和单药治疗组的中位缓解持续时间分别为30.4个月和12.9个月。治疗第24个月时,联合治疗组和单药治疗组分别有55%和35%的患者仍有缓解;治疗第36个月时,仅有联合治疗组有47%的患者仍有缓解。
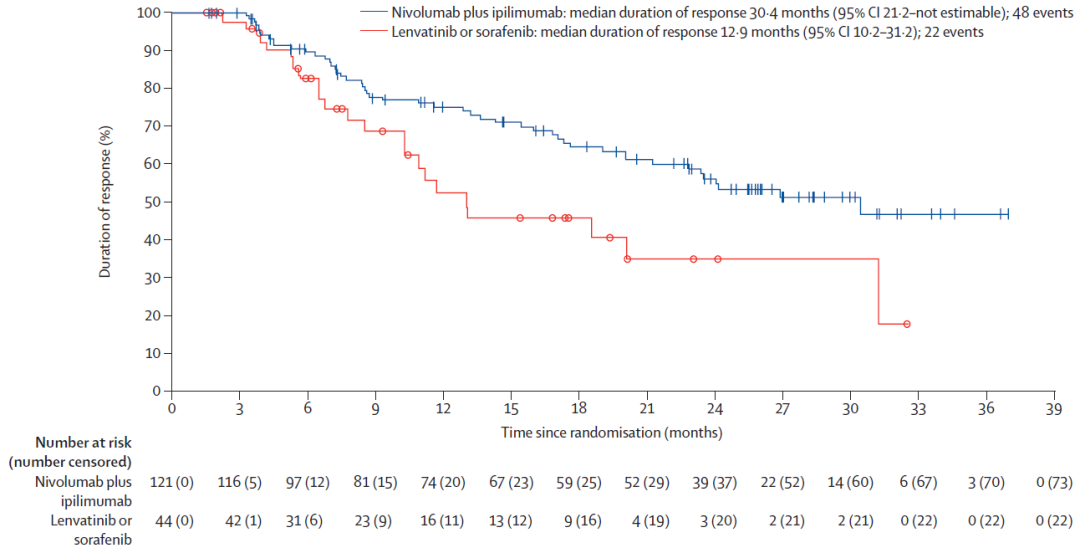
▲单药治疗组(红色)和联合治疗组(蓝色)持续缓解时间对比(图片来源:参考文献[1])
联合治疗组和单药治疗组中位无进展生存期(PFS)分别为9.1个月和9.2个月;18个月PFS率分别为34%和18%;24个月PFS率分别为28%和12%。
安全性方面,联合治疗组和单药治疗组分别有84%和91%的患者发生任何级别的治疗相关不良事件,两组3或4级相关不良事件的发生率相似(41% vs. 42%),与此前报道的该方案相关安全性特征一致。
总之,本次研究结果显示,对于既往未接受过系统性治疗的不可切除肝细胞癌,相较于TKIs靶向单药治疗,纳武利尤单抗联合伊匹木单抗的治疗方案可带来更好的生存获益,且这种获益在相关临床亚组中仍保持一致。
参考资料
[1] Thomas Yau, Peter R Galle, Thomas Decaens, et al. Nivolumab plus ipilimumab versus lenvatinib or sorafenib as first-line treatment for unresectable hepatocellular carcinoma (CheckMate 9DW): an open-label, randomised, phase 3 trial. Published Online May 8, 2025. The Lancet. Doi:10.1016/ S0140-6736(25)00403
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#肝细胞癌# #一线治疗#
16