读书报告 | 靶向B7H3的ADC在进展期实体瘤的I/Ib期研究
2025-07-23 iCombo iCombo 发表于上海
基于当前I/Ib的研究数据,YL201显示出总体可控的安全性及值得期待的疗效,期待规模更大的研究进一步验证其临床价值。
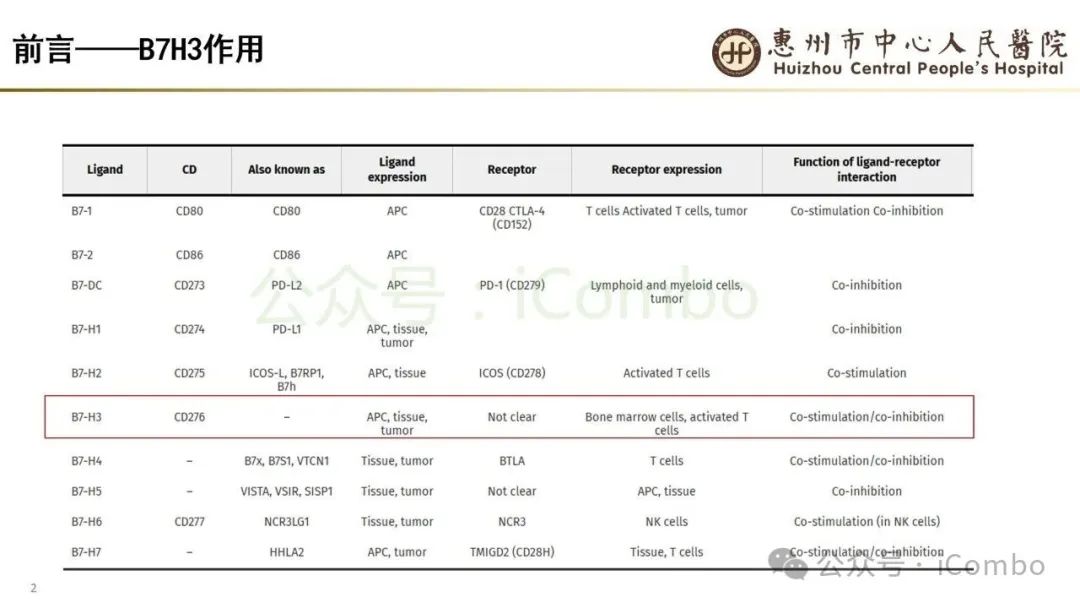
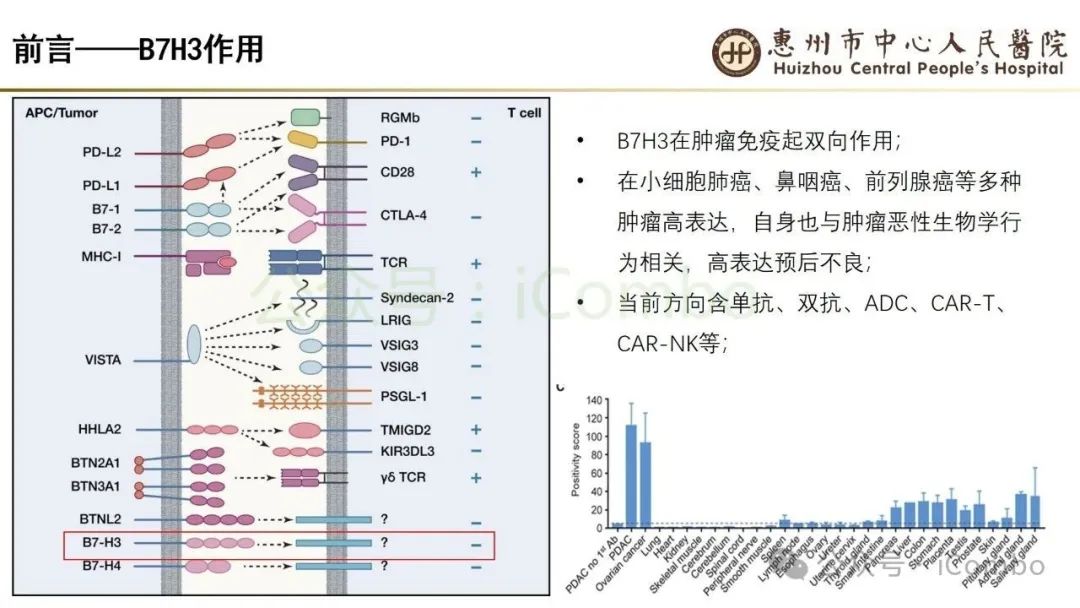
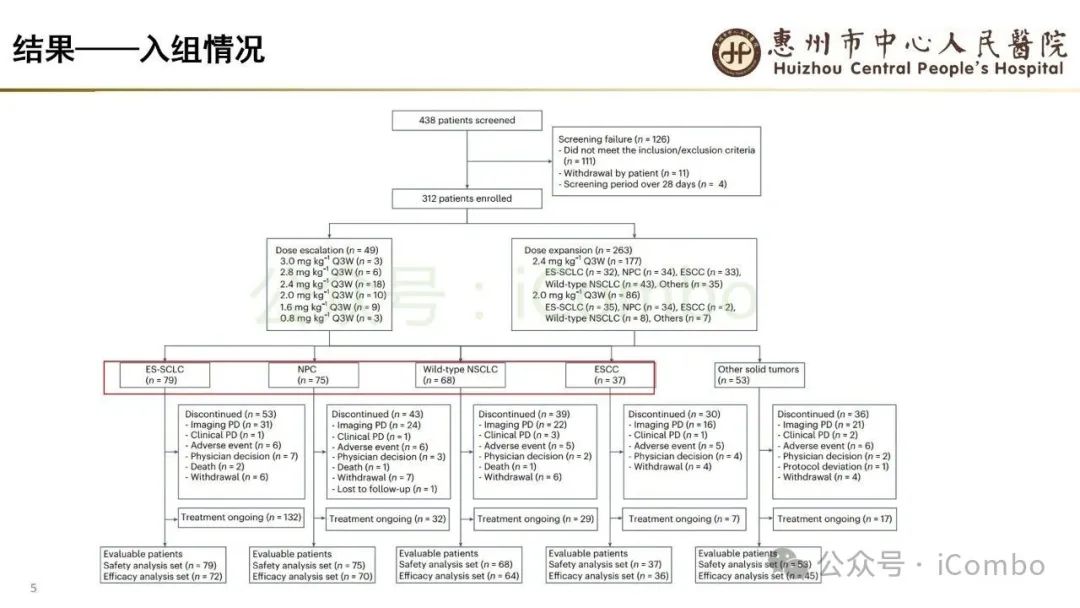
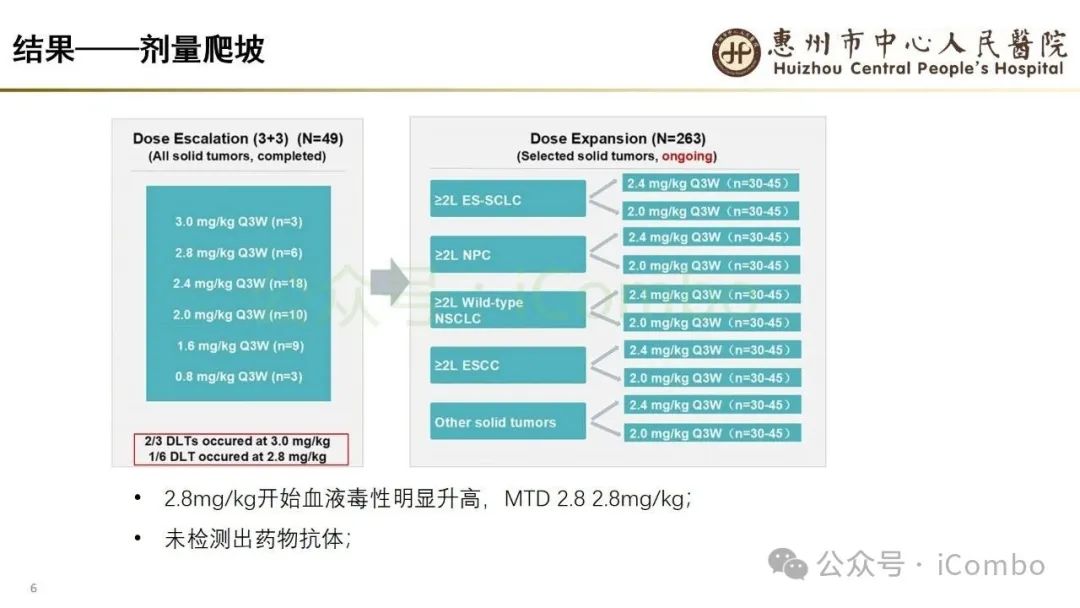
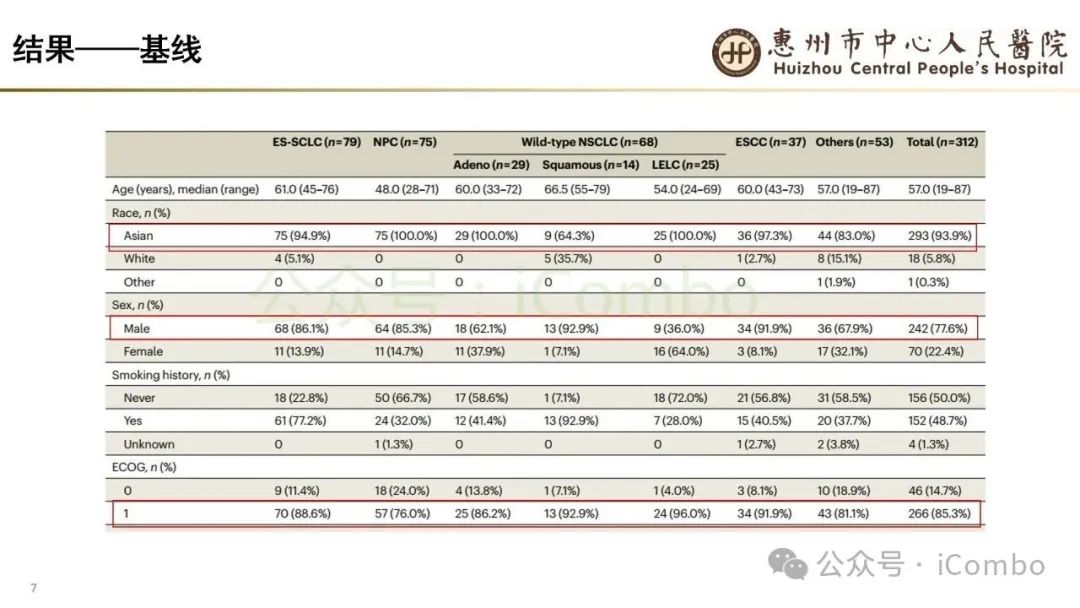
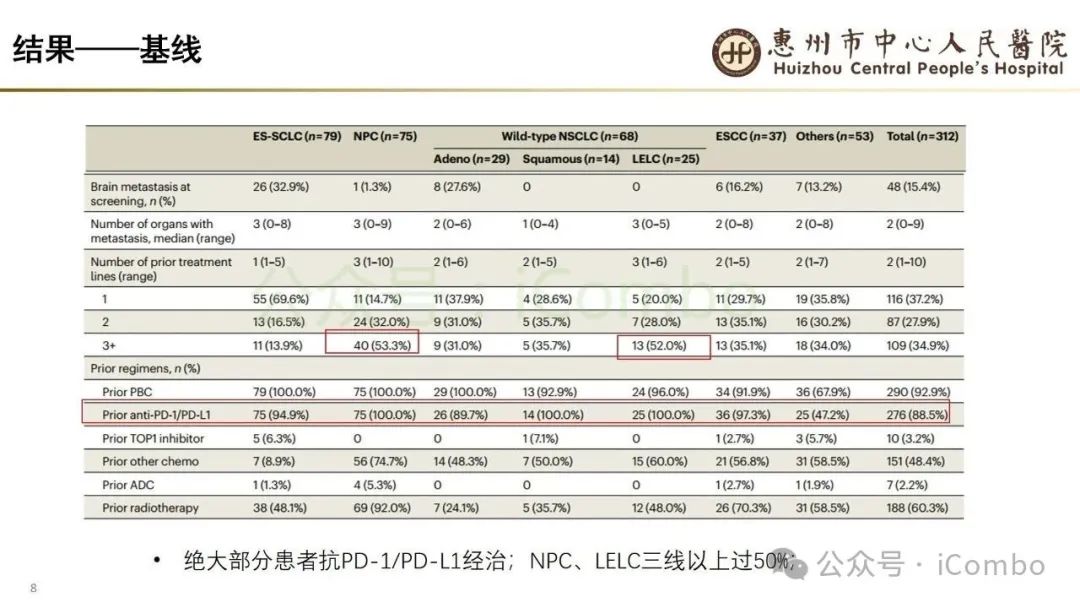
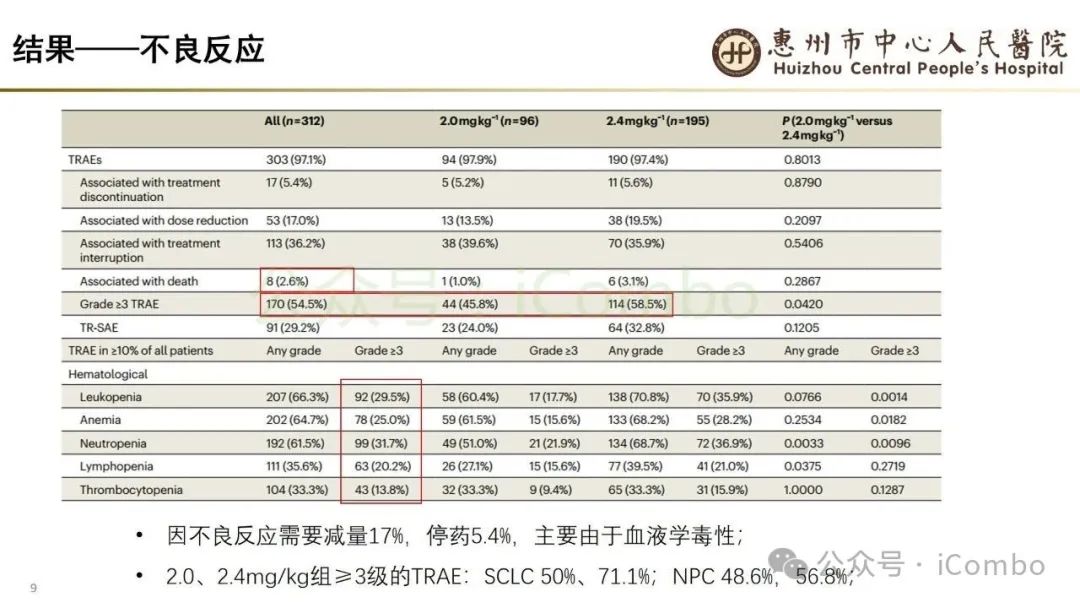
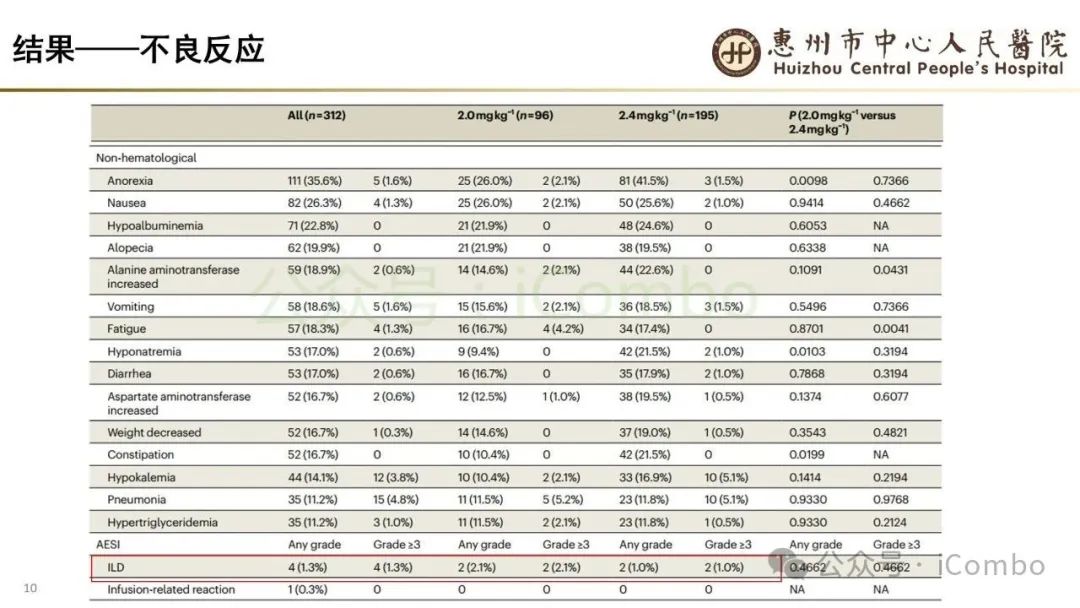
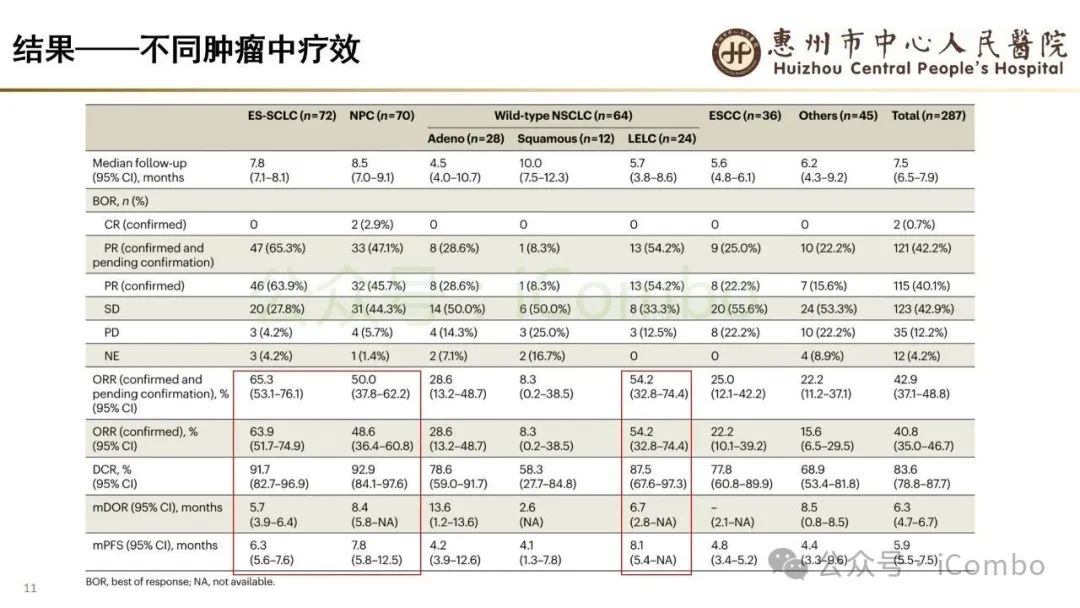
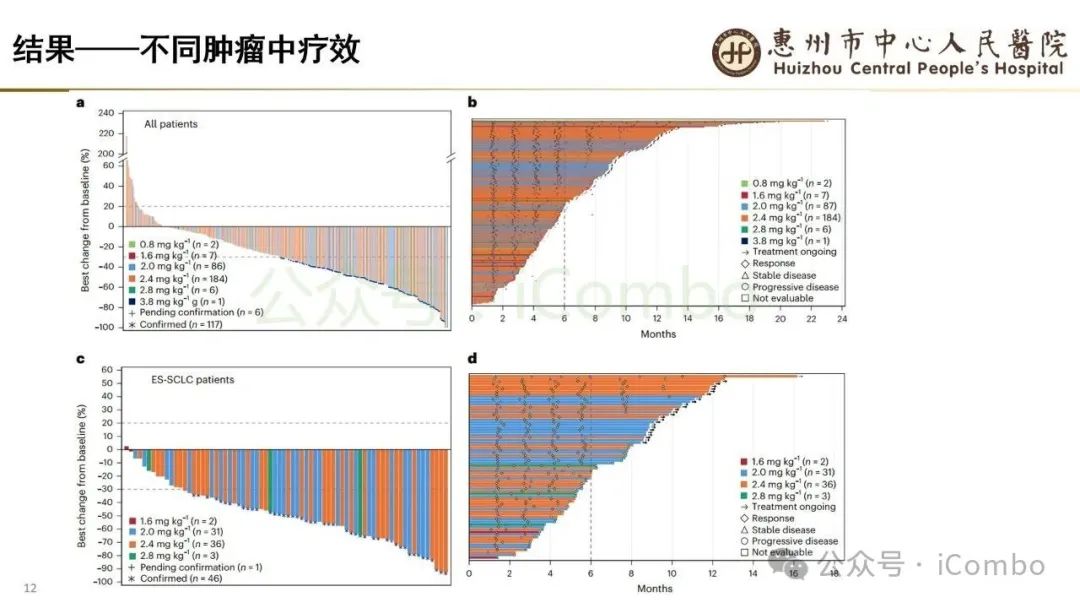
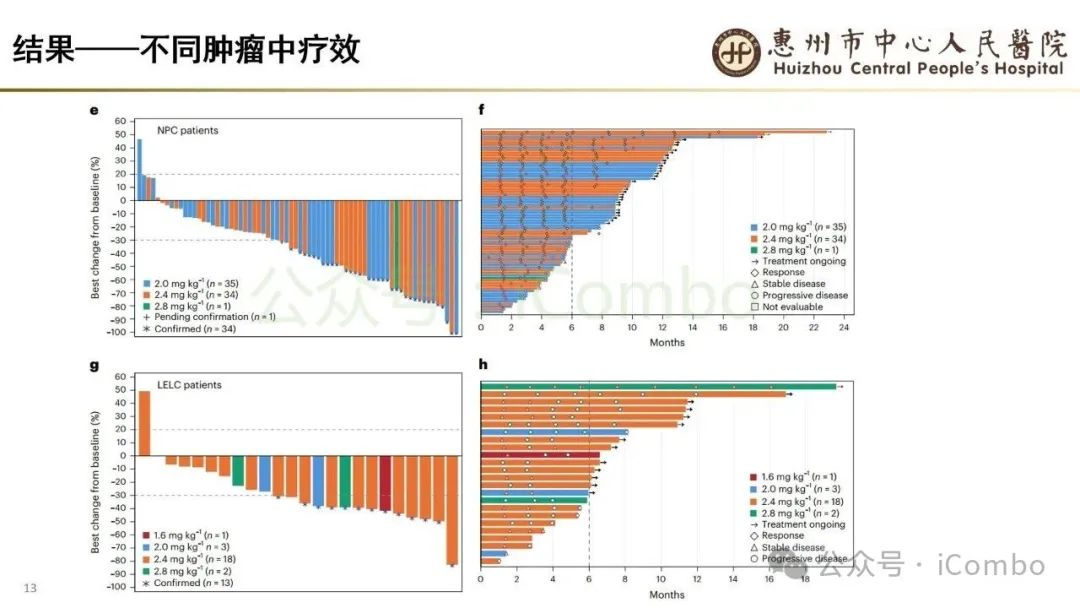
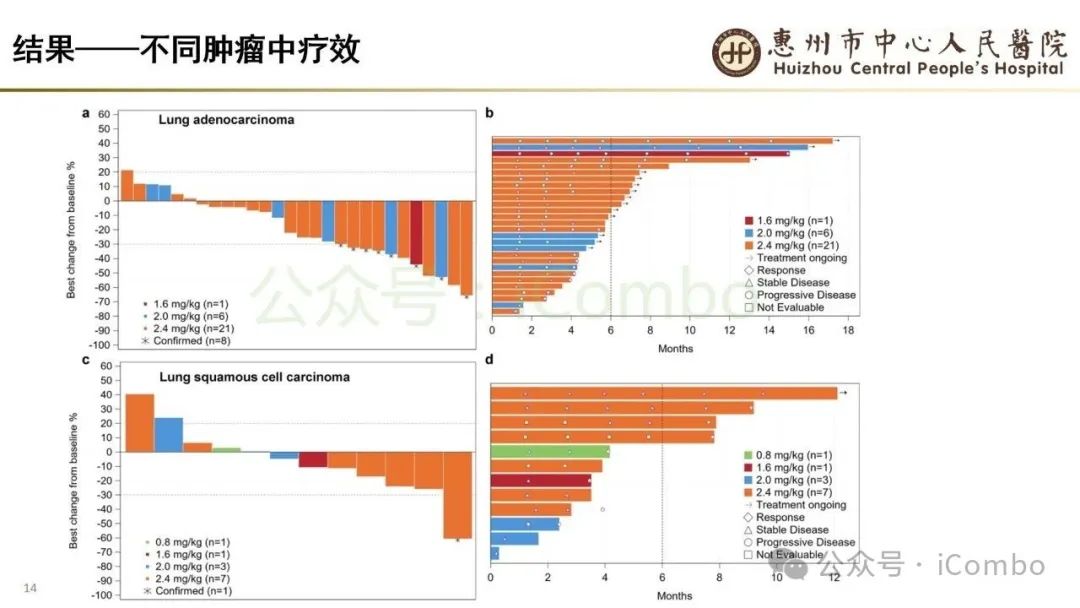
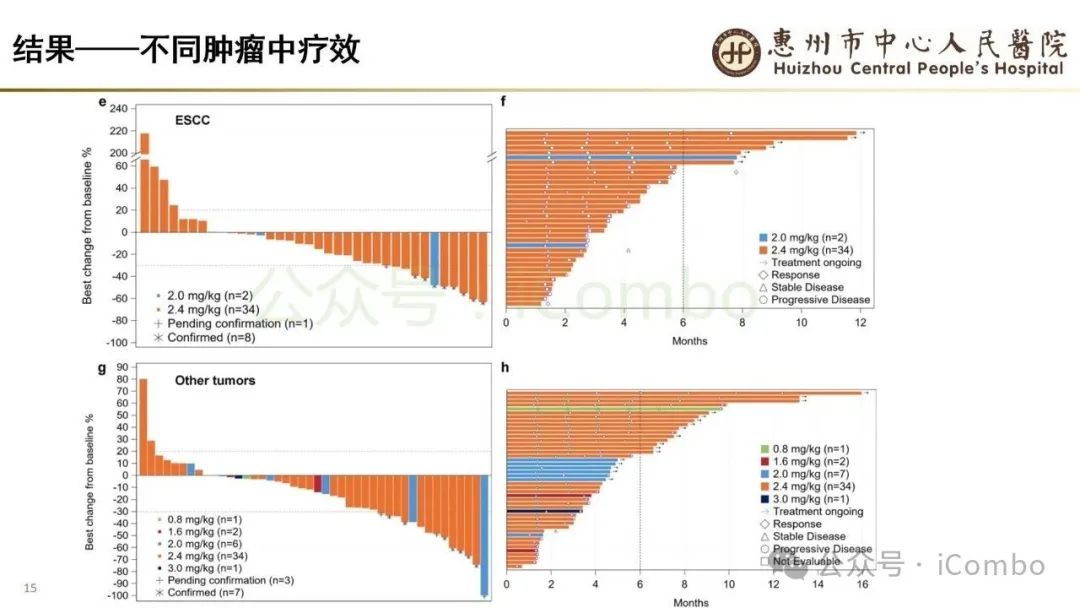
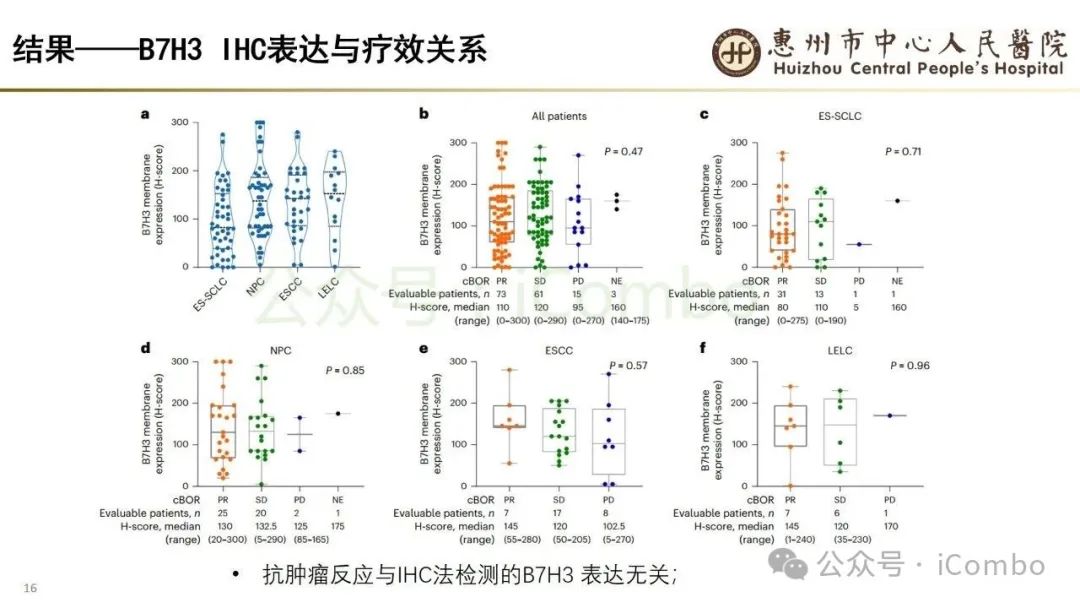
导读 当今抗体偶联药物(ADC)研究进展迅速,其中B7H3又是较有前景的靶点之一。B7H3在正常组织中表达相对较低,而在多种恶性肿瘤中呈现高表达,并参与诱导多种肿瘤恶性生物学行为,在免疫调节中起负性为主的双向作用。这些特征使B7H3成为ADC开发的理想靶点。本研究中,YL201是靶向B7H3的一种ADC,其载荷为YL0010014(拓补异构酶I抑制剂)。依靠自身平台的特殊链接子,YL201在体循环中更稳定,在肿瘤缺氧、酸性或溶酶体下易裂解释放高效载荷。 本研究未YL201用于多种进展期实体瘤的I/Ib期临床试验。纳入人群绝大部分均经过含铂化疗及免疫治疗。在鼻咽癌、淋巴上皮瘤样癌入组患者中,接受过3线及以上治疗的比例超50%。研究中最主要的不良反应为白细胞减少及贫血,而非血液学毒性不良反应为食欲下降;间质性肺炎总体发生率约为1.3%。从疗效上看,广泛期小细胞肺癌二线患者中,ORR仍高达65%,中位PFS为 6.5个月。在鼻咽癌、淋巴上皮瘤样癌中,ORR分别达48.6%及54.2%。且以上疗效未显示出对B7H3表达水平的依赖性。综上所述,基于当前I/Ib的研究数据,YL201显示出总体可控的安全性及值得期待的疗效,期待规模更大的研究进一步验证其临床价值(Nat Med. 2025 Jun;31(6):1949-1957. doi: 10.1038/s41591-025-03600-2)。


本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#实体瘤# #抗体偶联药物#
7 举报